论文总字数:19271字
目 录
第1章 绪论 1
1.1 水体中溴酸盐的来源与形成机理 1
1.1.1 溴酸盐的来源 1
1.1.2 臭氧氧化中溴酸盐的形成机理 1
1.1.3 溴酸盐的危害 2
1.2 溴酸盐的控制与去除技术 2
1.2.1 溴酸盐的控制技术 2
1.2.2 溴酸盐的去除技术 3
1.3 本论文的研究目的及意义 5
第2章 实验材料与研究方法 6
2.1 药品与设备 6
2.1.1 本实验中所用的化学试剂和药品 6
2.1.2 本实验中所用的仪器设备 6
2.2 吸附剂的预处理 6
2.3 表征方法 6
2.3.1 X射线衍射 6
2.3.2 Zeta电位 7
2.4 溴酸盐的吸附实验 7
2.4.1 溶液配制方法 7
2.4.2 pH-IS影响实验方法 8
2.4.3 吸附等温线实验 9
2.5 溴酸盐的分析 9
2.5.1 吸附后水样稀释 9
2.5.2 标准曲线的绘制 9
第3章 结果与讨论 11
3.1 吸附剂的形貌 11
3.2 吸附剂的表征 11
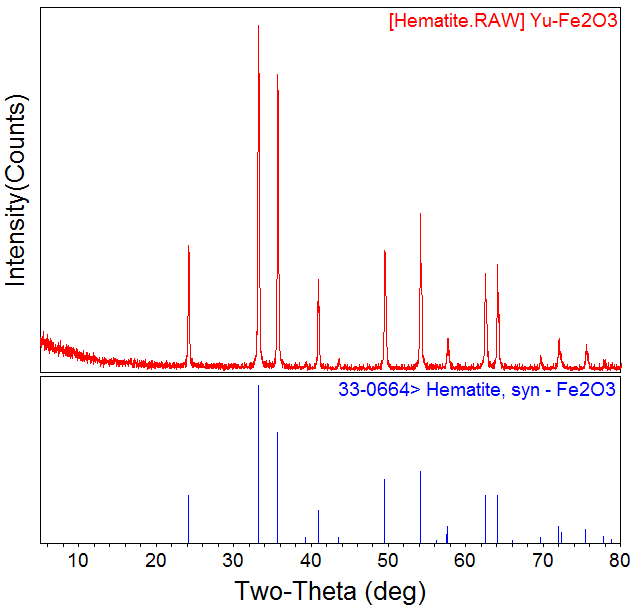
3.2.1 XRD 11
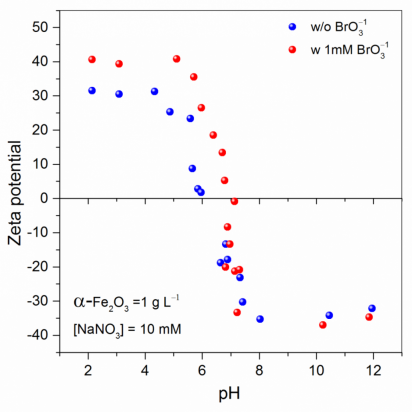
3.2.2 Zeta电位 12
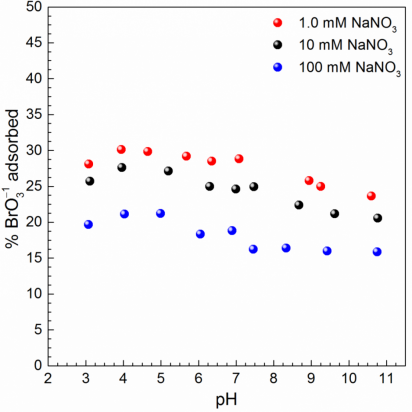
3.3 pH-IS影响实验 13
3.4 吸附等温线 13
第4章 结论与展望 18
4.1 结论 18
4.2 展望 18
参考文献 19
致 谢 21
赤铁矿对溴酸根离子的吸附行为研究
陈子琳
China
Abstract:The bromate derived from the ozonation disinfection of drinking water will have serious harm to people's health. So it has been a problem to remove the bromate in drinking water, which needs to be solved as soon as possible. Many domestic and foreign scholars have actively carried on research towards this problem and have explored several methods to control and remove the bromate in water. In this thesis, powdered hematite was used as adsorbent for adsorption of bromate. The effects of pH, background ionic strength, and temperature on the removal of bromate in water were also studied. The adsorption behavior of bromate on hematite was systematically analyzed. The removal mechanism of bromate on hematite and its possible industrial application was also discussed.
Key words: hematite; adsorption; bromate
第1章 绪论
1.1 水体中溴酸盐的来源与形成机理
1.1.1 溴酸盐的来源
水体中的溴离子(Br-)主要来自于海水入侵、矿物、沉积岩溶解、煤矿及钾矿的开发等,其本身对人体并无危害。一般,水体中溴离子(Br-)浓度低于20μg/L时,不会产生溴酸盐[2]。目前,饮用水的消毒常常采用的臭氧消毒法。作为替代氯消毒的水处理技术,臭氧消毒被广泛应用于给水废水的处理,它不仅能避免氯消毒过程中产生有毒害副产物,而且能有效去除水中有害物质。但是,臭氧消毒也有其弊端,当水体中含有溴离子(Br-)的浓度大于20μg/L时,在臭氧化过程中就会产生对人体有害的溴酸根(BrO3-)[2]。
1.1.2 臭氧氧化中溴酸盐的形成机理
研究表明,在臭氧氧化过程中溴酸盐有三条较为认可的生成途径:一是直接氧化途径(臭氧分子单独氧化)、二是直接-间接氧化途径(臭氧分子氧化-羟基自由基氧化)、三是间接-直接氧化途径(羟基自由基氧化-臭氧分子氧化)[3]。反应涉及到的溴元素价态多达6种,具体生成过程如图1.1所示。
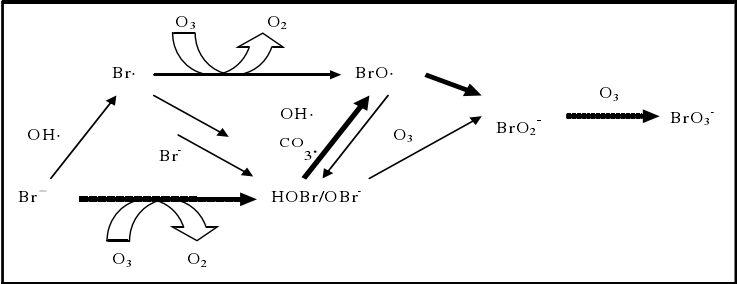
图1.1 臭氧氧化中溴酸盐生成过程示意图[4]
(1)臭氧分子直接氧化途径:
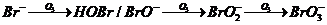 (1-1)
(1-1)
Br-逐步被O3氧化成BrO-,BrO2-,BrO3-。
- 直接-间接氧化途径:
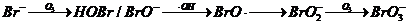 (1-2)
(1-2)
Br-先被氧化成BrO-,再和羟基自由基(·OH)反应生成BrO·,接着快速生成BrO2-, 再被O3氧化成BrO3-。
(3)间接-直接氧化途径:
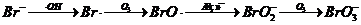 (1-3)
(1-3)
Br-先和羟基自由基(·OH)反应生成Br·,再逐步被氧化成BrO·和BrO2-,最后生生成BrO3-。
由此可见,水中溴酸盐的形成是 O3 和·OH共同发挥作用的结果,其生成与水中溴离子(Br-)浓度、臭氧投加量、pH值、有机物浓度及性质有着密不可分的关系。
1.1.3 溴酸盐的危害
饮用水中含有溴酸盐会对人体造成严重的健康威胁。溴酸盐被国际癌症研究机构(International Agency for Reserch on Cancer,IRAC)定为2B潜在致癌物,具有较高致癌可能性[1]。其致癌性和致基因突变性已在动物实验和微生物试验中得到证实。世界卫生组织(Word Health Organization,WHO)和美国环保局(United States Environmental Protection Agency,USEPA)作出规定,饮用水中溴酸盐最高允许浓度为10μg/L。我国《生活饮用水卫生标准》也规定,饮用水中溴酸盐的最高含量为10μg/L。因此,如何控制及去除水体中的溴酸盐越来越得到重视与关注。
1.2 溴酸盐的控制与去除技术
1.2.1 溴酸盐的控制技术
溴酸盐一旦形成,在水体中的性质很稳定,所以抑制溴酸盐形成的控制技术非常重要。目前常用的方法有降低pH值、加氨、优化臭氧投加方式、臭氧催化氧化等。
(1)加酸降低pH值
降低pH值可以减少溴酸盐的生成,原因如下:一、随着pH值的上升,O3分解产生更多的·OH,而·OH氧化生成BrO3-的速率比臭氧分子速率要快,因此,溴酸盐的产生量增加;二、降低pH值会减慢臭氧的衰减,增加臭氧分子的稳定性,同等条件下减少臭氧的投加量,从而一定程度上减少溴酸盐的产生;三、pH值的降低会使HOBr/BrO-的反应平衡向生成HOBr的方向移动,BrO-含量会降低,而臭氧氧化HOBr的速率远小于氧化BrO-,所以溴酸盐生成速率也会降低。
实验表明,pH值从8.0降到7.0,可以减少50%~66%的溴酸盐生成,但是此法只能用于低碱度的、或是在混凝前加酸可以达到强化混凝效果的原水,而且在实际应用中需要耗费大量的二氧化碳,不经济也不实用。
(2)加氨控制
水中加氨可以有效抑制溴酸盐的生成。当水中有氨存在,氨就会与HOBr反应生成溴胺,将生成溴酸盐的中间产物HOBr消耗掉,同时,氨与水中的·OH快速反应,从而减少溴酸盐的生成量。Siddiqui和Amy[5]实验表明,在1mol Br- 投加6.3mol的NH3-N可以较少65%的溴酸盐生成。Pinkernell等[6]发现,当水中的NH4 浓度增加到200μg/L(正常约为8μg/L)时,减少溴酸盐的生成达到50%,而继续增加NH4 浓度,溴酸盐的减少效果不明显。说明在一定程度上加氨能抑制溴酸盐生成,但是效果也有限。
(3)臭氧催化氧化
臭氧催化氧化可以去除在常温常压下臭氧氧化难以降解的有机物,提高臭氧氧化能力并提高臭氧的利用效率。不同的催化剂削弱BrO3-生成的效果也不同。何菇[7]等比较研究了在单独的臭氧氧化和有金属氧化物存在下的臭氧催化氧化中溴酸盐的生成情况,结果表明不同催化剂存在下臭氧催化氧化的效果大不相同,投入氧化镁和氧化铁会提高溴酸根离子的生成量,而氧化铈的存在可以抑制溴酸根的生成,因为氧化铈可以抑制臭氧氧化次氯酸从而抑制溴酸盐的生成。并且适当增加氧化铈的投加量,溴酸根的生成量随之降低:氧化铈投量为50mg/L时,溴酸根的生成量与臭氧单独氧化时减少了75.6%;在氧化铈含量从50mg/L增加至100mg/L过程中,可以发现,溴酸根生成量的减少率增加了6.2%;而当氧化铈投量超过100mg/L后,催化剂投量的增加对抑制溴酸根生成的效果并不明显。
(4)优化臭氧投加方式
剩余内容已隐藏,请支付后下载全文,论文总字数:19271字
相关图片展示:


该课题毕业论文、开题报告、外文翻译、程序设计、图纸设计等资料可联系客服协助查找;


