论文总字数:30746字
摘 要
氧还原反应在能源转化器件中有着非常多的应用,比如燃料电池、锌-空气电池等等。目前已经实现商业化的氧还原反应催化剂是Pt/C。但是其存在一些固有的缺陷难于克服,全球元素储量低、易于中毒,稳定性不高,环境不友好等等。
柚子皮是一种资源丰富的生物质材料,以它做氧还原催化剂的前驱体有着成本低廉、可持续、环境友好等一系列优点。并且,生物质独特的纤维素结构,为后期成碳材料的导电性打下良好的基础。最重要的是柚子皮是一种可以同时提供氮源和碳源的材料,避免了后期氮掺杂时使用其他无机材料或有机溶剂时对环境造成的不利影响。
在本文中我们以生物质为前驱体制备Fe, N-掺杂碳基催化剂,对柚子皮中加入的Fe元素含量和热解温度进行筛选,以期选定催化剂的最佳制备条件。同时采用扫描电子显微镜(SEM)、比表面积/孔径分析仪(BET)、能量分散谱(EDS)对催化剂的微观结构、表面形貌、元素组成和表面积进行表征。我们发现在Fe/柚子皮=0.1(质量比),热解温度为800度,N2气氛下保护时,制备的催化剂的氧还原性能最佳,并且在2000 s内的稳定性和抗甲醇毒化能力都超过了Pt/C。相比于不加铁的空白柚子皮,在相同条件下制备的催化剂来说,氧还原起峰电位提升了79 mV,证明柚子皮是一种有潜力的氧还原催化剂的制备前驱体,并且其制备的催化剂有可能代替Pt/C成为一种在汽车燃料电池阴极应用的新材料。
关键词:氧还原反应,生物质,柚子皮,燃料电池
Synthesis and electrochemical properties of carbon-based non-precious metal catalyst for oxygen reduction reaction
Abstract
Oxygen reduction reaction has many applications in energy conversion devices, such as fuel cells, zinc-air batteries and so on. Grapefruit skin is an abundant biomass material, which is of low-cost, sustainable and environment-friendly. Moreover, as a unique structure of biomass, cellulose lays a good foundation on conductive carbon materials, providing both nitrogen and carbon atoms which avoids the use of other inorganic materials and organic solvents.
In this thesis, we report a pathway to make Fe, N-doped carbon materials derived from grapefruit skin. The content of Fe and the pyrolysis temperatures was optimized. And, the SEM, BET, and EDS characterization help us to learn the surface morphology, elemental compositions and surface area of the catalysts.
It was observed that the best condition of making catalysts was using the Fe content of 10 at. %, the pyrolysis temperature of 800 oC under N2 atmosphere. Interestingly, the stability in 2000 s and the methanol poisoning capacity of the as-prepared catalysts were better than Pt/C. Therefore, grapefruit skin was a potential precursor of non-precious catalysts for oxygen reduction reaction and would replace Pt/C as cathode in fuel cells.
KEY WORDS: oxygen reduction reaction, biomass, grapefruit skin; fuel cells
目 录
摘要 I
ABSTRACT II
第一章 绪 论 1
1.1 引言 1
1.2 燃料电池 1
1.2.1 燃料电池的组成 1
1.2.2 减少燃料电池输出电压降的三个原因 1
1.3 氧还原反应 3
1.3.1 氧还原反应的发生过程 3
1.3.2 氧还原反应的应用 3
1.3.3 氧还原反应催化剂的发展历程 4
1.3.4 K-L方程 4
1.4 N-掺杂碳材料的概述 5
1.4.1 N-掺杂碳材料的制备方法 5
1.4.2 生物质碳材料的应用 6
1.4.3 N-掺杂碳材料的催化机理 7
1.5 本论文的研究背景及研究内容 8
1.5.1 研究背景 8
1.5.2 本论文研究内容及意义 8
第二章 以柚子皮为前驱体制备Fe, N-掺杂氧还原催化剂 9
2.1 试剂与仪器 9
2.2 实验操作步骤 9
2.2.1 Fe, N-掺杂催化剂的制备 9
2.2.2 测量方法 10
2.3 SEM测试和EDS测试 11
2.4 BET测试 13
2.5电化学性能分析 15
2.5.1 ORR测试 15
2.5.2 稳定性测试 19
2.5.3 甲醇毒化测试 20
第三章 总结与展望 21
3.1 总结 21
3.2 展望 21
参考文献(References) 23
第一章 绪 论
1.1 引言
燃料电池和普通的电池一样有着正负极和电解液,但是他实际上并不是一个储能装置而是一个发电装置,简单的说是一个能量转化装置。
燃料电池的阴极发生的是还原反应即氧气得到电子的过程。其中的电子转移过程是4e-转移。在得电子后其中的单质氧以-2价形式存在于物质中,碱性条件下的形式是OH-,酸性条件下以H2O的形式存在。现在燃料电池已经商业化的催化剂是Pt/C,但是Pt也因为存在储量低、成本高、选择性低、稳定性差、不利的环境影响等问题限制其发展。所以我们将目光聚焦在碳基催化剂上,相比于Pt,N-掺杂的碳基催化剂以其资源丰富、价格低廉、反应选择性高、催化稳定性好等优点成为科学家们的研究对象。因为上述的这些性能,N-掺杂碳基催化剂有望代替Pt在电化学催化氧还原反应方面的应用。但是还需要进一步优化合成策略,改变其石墨化程度来提高其催化性能。目前,在氧还原研究方面,N-掺杂碳基催化剂的催化机理尚不明确,对于哪种价键结构的氮起到了催化作用学界还没有明确的定论。
1.2 燃料电池
燃料电池不同于传统的能源转化器件。普通的能源转化器件比如内燃机是通过化学能转化为热能再通过做功的方式产生电能的方式实现能源转化的。不受卡诺循环限制的燃料电池可以直接将化学能转化为电能,理论能量转化效率可达100 %,所以作为一种环境友好的能源转化器件,其发展备受大家的广泛关注。
1.2.1 燃料电池的组成
应用在汽车上的燃料电池一般是通过氢气的电化学氧化生产电量的。相同的重复单元电池是燃料电池组成的基本结构,其中包括膜电极组件(MEA)。在膜电极组件的阳极上氢气(H2)被氧化,阴极上氧气(O2)被还原,如图1-1所示。所有的器件及相关过程都被压缩在两块平板之间,包括引入气体反应物和冷却剂到膜电极组件的过程。电化学反应发生在膜电极组件的电极上,通过固体聚合物离子交换膜传递的是质子而不是电子。阴极和阳极的反应是发生在不同的Pt基催化剂表面上的,在阴极氧气被还原,在阳极氢气被氧化。纯水和热量是仅有副产物。其中存在的多孔气体扩散层不仅在溶液和催化剂表面发生物质交换,传递反应物和产物水,而且还是两者交换电子的媒介。
1.2.2 减少燃料电池输出电压降的三个原因
膜电极组件的性能通过三点得到体现,分别是输出电压、电流密度和如图1-2所示的极化曲线。当电流通过电池时,有三个主要原因造成能量损失从而导致电压降低:阴极氧还原反应的动力学反应,因为材料和电极表面存在电阻造成的损失(iR),由于催化剂不能获得足量的氧气并且在高电流密度时的质量传递产生的超电势。从图2的极化曲线可以发现,理论的起峰电位(零电流)是1.169 V;记录下的起峰电位是低于理论起峰电位的,这是由于气体不能被膜完全分离和有限的电子阻力造成的。所测量的电池电阻乘以电流密度可以得到iR损耗,这可以被添加到所测量的极化曲线(蓝色)中,得到消除内阻降后的极化曲线(红色)。消除内阻降后的极化曲线与理想动力学曲线之间的差别就是所有质量传递损失的总和。在实际的电流密度范围内,改善膜电池组件的电阻可以比改善动力学对实际的电池电压具有更大的影响。因此电池电阻也一直都被研究,并且已经减少到远远小于膜和气体扩散介质对于输出电压降的影响。对于解决动力学损失可能更具挑战性,因为氧还原反应动力学数量级的提高而使起峰电位提高的幅度也只在60-70 mV左右,至今催化剂的开发进度也只取得电池电压几十毫伏的提高,但是对于消除超电势的影响要提升相同的几十毫伏也是困难重重。
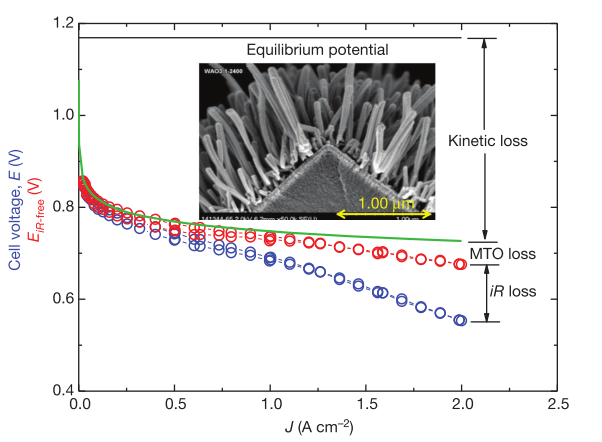
图 1-1 燃料电池的极化曲线[1]。测量的燃料电池中Pt族金属膜电池组件极化曲线(蓝色)。消除内阻降后的极化曲线(红色)相比于理论上只有动能损失的曲线(绿色),他们之间的差别是由于超电势的质量传递。极化曲线是基于NSTF PtCoMn催化剂的膜电池组件在150 Kpa 氢气/空气下测量的。
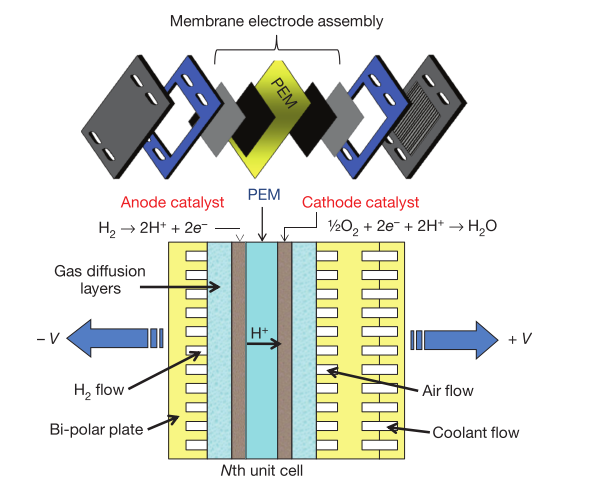
图 1-2 燃料电池的组成[1]。燃料电池堆中第N个单元电池的横截面,该图展示的是一个扩大的膜电极组件
燃料电池想要商业化必须满足三个基本标准:成本,催化性能和稳定性。阴极发生的氧还原反应速率比阳极的氢氧化反应速率慢6个数量级,因此限制了燃料电池的性能,所以所有的研究和发展,都着眼于提高阴极的催化剂和电极。大部分的膜电极组件催化剂都是基于Pt(以纳米粒子的形式分散在炭黑负载上),其中贵金属的高昂的价格,严重影响了成本。经美国能源部的车队测试,汽车燃料电池的阴极的Pt负载量要达到0.4 mg Pt cm-2,在这些汽车中催化剂/膜电池组件的稳定性目标已经缩减到5000小时。如何通过把Pt负载减少到0.1 mg Pt cm-2以下来减少成本但又不降低性能或者是稳定性是大部分电化学催化研究的课题。目前美国能源部2017年的对于整个Pt族金属(阴极 阳极)的电化学性能的目标是在膜电极组件上利用0.125 mg Pt cm-2来产生额定功率堆密度为8.0 KW g-1 Pt。每辆汽车8 g的Pt族金属的负载产生的功率与现在的内燃机是一样的。
要满足车辆操作的基本条件,对于ORR催化剂的的稳定性和催化活性还有更进一步的要求。系统集成要求膜电极组件在0.6 V的电压下电流密度不低于1.5-2 A cm-2,这是由于散热器尺寸和相关冷却装置的限制。催化剂必须承受成千上万次的循环、启动和熄火操作,达到5000小时的使用期。根据查阅文献可知,Pt/C催化的起峰电位的升高趋势是性能退化的主要表现,甚至是短时间内H2/空气波在流场中启动和关断都会对其性能造成影响。一些正在开发的对策是使用更加稳定的石墨化碳材料,负载在不会发生电化学腐蚀的催化剂载体,并且加入析氧催化剂的组合以在水被氧化开始之前夹紧电位[2, 3]。
1.3 氧还原反应
1.3.1 氧还原反应的发生过程
选择性高的催化剂的发展对于了解靶向催化剂的电化学氧气还原成水的细节是有帮助的。,这是一个机理非常复杂的反应。这通常包括不同的反应路径,例如直接的4e-转移过程将吸收的氧气变为水,或者是2e-转移过程将吸收的氧气先变为H2O2再接受另外的2e-变为水。不管机理的细节,动态电流密度i,通过Pt电极表面标准化后产生的电势E[3],已经被应用在吸收吉布斯能的计算中。
(1)
在这里n,F,xR都是常数,是氧气的摩尔浓度,是电极表面气体的吸附分数。
在(1-)的指前因子发展的过程中,关键一步的假设是发生氧还原反应时其控制步骤是电子第一次转移的步骤,Pt Pt,并且氧气吸附的表面的杂质是羟基,而不是活性中间体。这表明,任何影响到表面原子或电子结构延缓羟基吸附并阻止氧气吸附位点的改变都会对特定活性具有积极的影响。因为在公式(1)中(1-)会变得更大。这种模式支持用于提高氧还原反应催化活性中电化学催化的方法,但是最近的一些模型计算和测量中认为将附的氧或羟基物质比中间体扮演一个更积极的角色[1]。
1.3.2 氧还原反应的应用
很多的电化学器件中都会涉及氧还原反应,比如燃料电池[1],锌空气电池[4],同时氧还原反应还有一些其他的应用包括水净化,氧气检测和防腐蚀保护[5]。目标上我们的氧还原催化剂都选择性的完成氧还原反应的4e-转移过程,但是也可以利用碳材料选择性催化2e-转移过程来生产H2O2。Chen等人[6]发现了一种多孔层次碳材料可以选择性的催化H2O2的生成。在传统的工业中蒽醌法被广泛用于生产过氧化氢,但是备受环境保护问题的争议,而电化学还原氧气的方法又是不经济的。所以该课题组发现了一种多孔层次碳材料(HPC)来还原氧气,产生过氧化氢的选择性可以达到95.0 %-70.2 %。并且在PHgt;1-4时,大部分催化剂的选择性在90.0 %以上,在PH=7时,大部分催化剂的选择性在80.0 %以上。在PH=1-7,电压为-0.5 V的条件下,2.5小时内过氧化氢浓度可达222.6-62.0 mmol L-1,过氧化氢的产生速率可达395.7—112.2 mmol h-1 g-1。而且对于HPC对电化学合成过氧化氢有如此出乎意料的效率可以归功于高含量的sp3-C和结构缺陷,大的表面积和快速电子转移。
1.3.3 氧还原反应催化剂的发展历程
1.3.3.1 Pt材料和Pt合金材料
对于Pt和Pt合金材料来说,在催化氧还原反应时中存在一些缺陷。比如全球储量较低导致Pt的价格比较昂贵,在应用时成本较高。易于中毒,在氢气燃料电池中,主要发生的是对于一氧化碳的中毒反应,这是由于工业中的氢气的生产过程是伴随着合成气的生产过程的,在其中必然会有较低浓度一氧化碳的残留,在燃料电池中就会通过质子交换膜到达阴极慢性导致Pt的中毒。在甲醇燃料电池中,主要发生的是对于甲醇的中毒反应,燃料甲醇从阳极通过质子交换膜到达阴极导致催化剂中毒。低稳定性,Pt和Pt合金材料在氧还原反应催化是随着时间的增长会发生催化能力的降低,比如在旋转环盘测试中,Pt和Pt电极连续工作2000 s之后,电流密度就会衰退到起始电流密度的93.68 %。他们有如下集中分类:
剩余内容已隐藏,请支付后下载全文,论文总字数:30746字
相关图片展示:




该课题毕业论文、开题报告、外文翻译、程序设计、图纸设计等资料可联系客服协助查找;


