论文总字数:22447字
摘 要
本文采用等体积浸渍法分别制备了以乙二胺合镍、硝酸镍和醋酸镍为前驱体负载在活性炭上的3种不同催化剂。在大气压力、400/500℃条件下,在固定床反应器上进行HI催化分解反应,以评价不同前驱体制备的Ni/AC催化剂的性能。通过氮吸附仪(BET)分析、X-射线衍射(XRD)分析和透射电镜(TEM)分析等多种测试方法对反应前后催化剂的结构特点进行了表征。催化剂活性评价的结果表明,以醋酸镍为前驱体制备的Ni/AC催化剂具有最高的催化活性,400℃、500℃下催化HI转化率分别为13.61%和23.9%,而以乙二胺合镍为前驱体制备的Ni/AC催化剂具有最低的催化活性,400℃、500℃下催化HI转化率分别为4.89%和11.83%。不同前驱体制备的Ni/AC催化剂活性差异较大,这可能是因为不同的镍盐与活性炭之间的相互作用强度不同。醋酸镍与活性炭的相互作用较强,浸渍时更易充分吸附在活性炭表面上,经还原后,镍颗粒在负载表面分布较均匀且晶粒较小。
关键词:镍盐前驱体;活性炭;热化学制氢;硫碘循环;碘化氢分解;催化剂
Abstract
Equivalent-volume impregnation was applied to prepare different Ni/AC catalysts, whose precursors were nickel ethylenediamine, nickel nitrate and nickel acetate, respectively. Under the condition of atmospheric pressure and temperature of 400/500 ℃, the reaction of HI decomposition was conducted in a fixed bed reactor to evaluate the catalytic performances of these catalysts. In order to characterize the different catalysts before and after HI decomposition, testing methods of BET, XRD and TEM were used. The results of activity evaluation indicated that Ni/AC catalyst prepared from nickel acetate showed the best catalytic activity for HI decomposition, with a HI conversion of 13.61% at 400℃ and 23.9% at 500℃. Meanwhile, Ni/AC catalyst prepared from nickel nitrate showed the worst catalytic activity, with a HI conversion of 4.89% at 400℃ and 11.83% at 500℃. Catalytic activities of these three Ni/AC catalysts varied a lot, which may resulted from the interaction of nickel salts and active carbon support. Interaction between nickel acetate and active carbon was strong enough to make nickel acetate molecule easily be absorbed on the surface of active carbon. Therefore, the nickel crystallites on the surface of active carbon showed better dispersion and smaller size.
Key words: nickel salts precursors; active carbon; thermochemical hydrogen production; iodine-sulfur cycle; HI decomposition; catalyst
目 录
摘要 I
Abstract II
第一章 绪论 1
1.1 研究背景及意义 1
1.2 制氢方法简介 2
1.2.1 化石能源制氢 2
1.2.2 生物质制氢 3
1.2.3 水制氢 4
1.3 热化学硫碘循环制氢 4
1.3.1 热化学硫碘循环制氢简介 4
1.3.2 热化学硫碘循环制氢过程中HI分解催化剂的研究进展 5
1.3.3 热化学硫碘循环制氢过程的研究趋势 7
第二章 实验方法概述 7
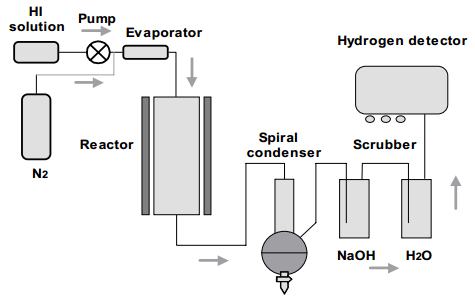
2.1 HI催化分解实验系统 7
2.2 催化剂的制备 9
2.2.1 活性炭预处理 9
2.2.2 等体积浸渍法 9
2.2.3 还原法制备Ni/AC 10
2.3 催化剂的活性评价 10
2.4 催化剂的表征 10
2.4.1 氮吸附仪(BET)分析 10
2.4.2 X-射线衍射(XRD)分析 11
2.4.3 透射电镜(TEM)分析 11
第三章 三种不同镍盐前驱体制备的Ni/AC 11
3.1 三种镍盐前驱体 11
3.1.1 前驱体种类的选择 11
3.1.2 前驱体的获得 12
3.2 催化剂的制备 13
3.3 催化活性比较 13
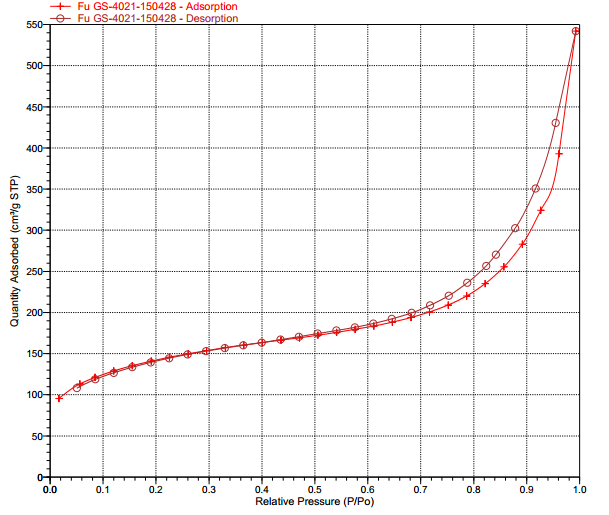
3.4 BET分析结果 14
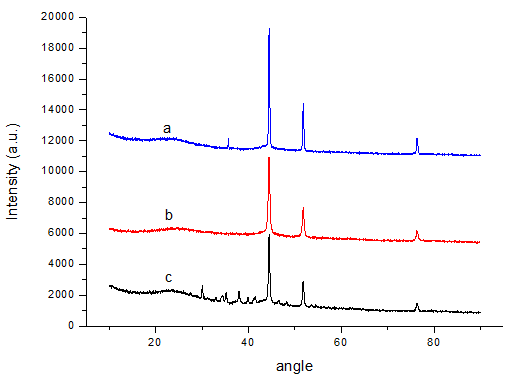
3.5 XRD分析结果 16
3.6 TEM分析结果 18
第四章 总结与展望 21
4.1 总结 21
4.2 展望 23
参考文献 24
致谢 26
第一章 绪论
1.1 研究背景及意义
能源是人类社会赖以生存的基础。各种能源中,尤其以化石能源的利用最为广泛,极大地推动了社会发展,人们的生活水平得以提高。但是,地球上的化石能源储量有限,寻找新型的替代能源迫在眉睫。而另一方面,由化石燃料利用产生的等温室气体和、等污染性气体,严重破坏了生态环境,威胁到人类的生存[1]。面对化石能源短缺和生态环境污染的双重压力,我们必须找到一种清洁、安全、高效、可持续的替代能源。氢能由于具有上述优越的性质,能够缓解能源危机的巨大压力,越来越引起人们的关注。
制氢方法多种多样,目前国际上主要的制氢方法有:化石能源制氢、生物质制氢、水制氢[1]。化石能源制氢虽然技术简单、氢产量稳定,但仍然依赖煤等化石燃料,且制氢过程存在一定的污染,目前作为过渡工艺采用,将来会逐步被淘汰。生物质制氢技术起步较晚,大多还停留在实验阶段,需要进一步的深入研究。水制氢技术包括电解水、光解水、高温热解水、热化学循环水分解等多种方法。经评估[3-6],热化学硫碘循环水分解制氢技术具有循环反应数较少、热效率较高、环境安全、操作简便等优点,是制氢的理想循环,有深厚的研究基础。基础研究发现,硫碘循环中经HI分解才可得到氢气,故HI的转化率对氢气的产率有很大的影响。如果不使用催化剂,HI的分解率会很低。因此,在实际应用中,必须通过使用催化剂来提高HI转化率,从而达到提高氢产量的目的。通常采用Pt、Pd、Ni等过渡金属负载在不同的催化载体上构成催化剂[7]。虽然Pt基催化剂具有很好的催化活性,但考虑到原料成本,需加快对非贵金属类高活性催化剂的研究开发。本文采用不同前驱体制备Ni基催化剂,比较它们在HI分解反应中的催化活性,并利用BET、XRD、TEM等多种分析方法对反应前后的催化剂形态进行表征,从而筛选出较好的催化剂,以达到降低反应成本、优化硫碘循环制氢过程的目的。
1.2 制氢方法简介
制氢方法多种多样,目前国际上主要的制氢方法有:化石能源制氢、生物质制氢、水制氢[1]。其中,生物质制氢和水制氢利用的是可再生能源,符合可持续发展战略,是未来发展的方向。
1.2.1 化石能源制氢
化石能源制氢的原料来源十分广泛,包括煤,天然气、煤层气等气体化石燃料,轻质油、重油等液体化石燃料[2]。
(1)煤制氢技术
煤制氢技术是目前使用最为广泛的制氢技术,一般通过煤的焦化和煤的气化来制取含有氢气的多种可燃气体。
煤的焦化又称煤的高温干馏,它是以煤为原料,在隔绝空气的条件下,将煤加热到接近1000℃,从而通过高温干馏生产焦炭,同时获得焦炉煤气。煤焦化获得的主要产品焦炭,可以用于炼铁、制造电石和电极等方面,是十分重要的化工原料。副产品焦炉煤气是含有氢气的混合气体。通常情况下,焦炉煤气中氢气体积含量约为57.5%、甲烷体积含量约为25%、一氧化碳体积含量约为6.5%。除了前述几种可燃气体,焦炉煤气中还含有氨、苯、甲苯、二甲苯、硫及硫氰化合物等多种物质,通过吸收、分离等手段回收这些物质,可用作化工工业的重要工业原料,也能在一定程度上减少焦炉煤气后续利用过程中对环境的污染。经分离处理过后的焦炉煤气可以用作城市煤气或工业用气体燃料。相对于直接燃烧煤,将焦炉煤气用作气体燃料更干净清洁。
煤的气化是指在一定温度和压力下,煤与气化剂在特定的反应器内发生一系列的化学反应,将固体煤转化为含有氢气的多种混合气体的过程。常用的气化剂有空气、水蒸气和氧气等气体。特定的反应器称为气化炉,根据气化炉内煤与气化剂的接触方式可将常用气化方式分为固定床气化、流化床气化、气流床气化和熔浴床气化等。根据所用气化方式的不同,煤气化后所得混合气体中,各气体组分的含量也大不相同。通常将气化所得的氢气。甲烷等可燃气体称为煤气,而氨等可作化工原料的气体称为合成气。煤气可用作钢铁、机械等工业部门的加热燃料,也可用作民用燃料。和利用焦炉煤气相似,气化得到的煤气用作燃料与直接燃煤利用热量相比,前者更加清洁,能减少煤中有害物质对环境的污染,大大提高了煤的利用率。
我国是一个燃煤大国,煤储量丰富,在未来很长一段时间内,煤将仍然是我国能源结构的主要部分。因此,煤制氢技术是符合我国国情的便捷可行的制氢方法。在我国,目前已建有大量煤制氢的工业装置。煤制氢方法技术成熟、操作简便、成本相对较低,但仍然依赖储量有限的化石燃料,且制氢过程存在一定的污染,目前作为过渡工艺采用,将来会逐步被淘汰。
(2)气体化石燃料制氢
气体化石燃料主要包括天然气和煤层气,而在制氢中应用较多的是天然气制氢,其制氢方法主要有:天然气水蒸气重整制氢、天然气部分氧化重整制氢、天然气水蒸气重整与部分氧化联合制氢、天然气(催化)裂解制氢[2]。天然气水蒸气重整制氢的研究已有近百年的历史,经过不断的实践与改进,已形成了多种制氢工艺,在工业上得到广泛应用。其制氢流程基本为:天然气与氢气以一定的比例相混合,被加热至一定温度之后,在金属催化剂的催化作用下发生加氢反应,再进入蒸汽转化炉进行甲烷水蒸气重整制氢反应。该制氢方法反应条件较容易控制,获得了广泛的应用。天然气部分氧化重整制氢方法能耗更低,但反应条件过于控制,在实际应用中难以控制,且反应需要大量纯氧,使得成本增加。天然气(催化)裂解制氢是一种新型天然气制氢方法,不会产生二氧化碳排放,碳元素转化为、固体碳,具有很高的经济效益和环境效益。
(3)液体化石燃料制氢
常用的用于制氢的液体化石能源包括甲醇、乙醇、轻质油和重油等。制氢技术有甲醇裂解-变压吸附制氢技术,轻质油与重油的催化分解制氢技术等,催化剂在这些制氢技术中均发挥了重要作用。
1.2.2 生物质制氢
地球上的生物质资源十分丰富,生物质能是一种洁净安全的可再生能源,但其作为能源不能直接应用于工业设备,需要通过一些手段转化为其它可利用的能源。目前的生物质制氢技术主要可分为生物质热化工转化制氢和微生物制氢[8]。生物质热化工转化包括生物质的气化、热解等技术,将生物质转化为可燃气体、生物油等可大规模利用的能源。微生物制氢技术通过光合细菌的光合生长和藻类的氢代谢,能够源源不断的产出氢气。生物质制氢是一项很有发展前景的技术,但是这种制氢技术起步较晚,大多还停留在实验阶段,需要进一步的深入研究。
1.2.3 水制氢
以水为原料的制氢技术可分为电解水制氢、光催化分解水制氢、直接热分解水制氢和热化学循环水分解制氢[9]。
电解水制氢技术原理简单,它将一对浸没在电解液中的电极通入直流电,水就被分解制得氢气。电解水制得的氢气纯度很高,且该反应过程简单、无污染。但同时,电解水需要消耗大量电能,考虑到火力发电的效率并不高,故电解水制氢过程的能源利用率较低,出产等量的氢气要耗费更多的能量,一般在对氢气纯度要求高的情况下采用。
光催化分解水制氢是向水中加入某些能吸收太阳能的物质,这些物质吸收光能后再传递给水分子,使其分解产生氢气。如果要使光解水制氢投入工业应用,就必须要开发高效的催化剂和建立稳定高效的催化体系。
直接热分解水制氢的原理十分简单:将水加热到一定温度使其裂解生成氢气和氧气。该反应是一个很强的吸热反应,需要强大的热源加热水至3000℃以上才能使水大量分解,目前认为合适的热源只有太阳能和核聚变热。且在高温下,选择合适强度的材料、实现氢与氧的分离等都是亟待攻克的技术难关。
热化学循环水分解制氢是通过一系列相关联的化学反应将水分解制得氢气,整个过程除了消耗水和一定能量,其它添加的物质均不消耗,构成一个封闭的循环。由于将水分解反应分解成几步反应,它的反应温度要低于直接热分解水制氢,且该循环过程效率较高,无碳排放,是一种较佳的制氢方法。热化学循环制氢法中使用的循环多种多样,一般根据反应所涉及的物料种类,主要可分为:卤化物体系、含硫体系、氧化物体系、杂化体系等[2]。本文研究的则是含硫体系中的硫碘循环(SI或IS循环)。
1.3 热化学硫碘循环制氢
剩余内容已隐藏,请支付后下载全文,论文总字数:22447字
相关图片展示:
该课题毕业论文、开题报告、外文翻译、程序设计、图纸设计等资料可联系客服协助查找;