细胞表面分级石墨烯的构筑及增强电性能毕业论文
2020-04-05 10:45:20
摘 要
细胞表面包覆是指通过材料与细胞的交互作用使材料包覆细胞并使细胞表面功能化的过程。这一方法在生物医学上有诸多运用,同时也可以利用细胞包埋设计生物细胞传感器、热化学传感器、仿生传感器等生物电子设备。其中细胞电极有着极其广泛的作用。为了研究并设计细胞电极,本文利用细胞包埋技术对酵母细胞表面进行修饰,从而增强其电学性能并争取有所突破。石墨烯因其优异的电学性能受到了广泛的关注,因此本文尝试在酵母细胞表面包覆一层石墨烯片层以增强细胞导电性。用氨基苯硼酸将酵母细胞表面进行修饰后,用化学还原法还原的氧化石墨烯可以包覆在细胞表面以形成导电界面。以还原氧化石墨烯沉积在细胞表面得到的包覆壳层有着很好的生物相容性,被包覆的细胞仍能进行正常的生理活动并且包覆过程对细胞的损伤很小。同时本文还尝试将还原氧化石墨烯片层与金纳米颗粒混合以得到担载了金纳米颗粒的还原氧化石墨烯片层,以这一复合材料包覆细胞,可以更为明显的增强细胞的电学性能。
关键词:石墨烯;单细胞包覆;分级结构;酵母细胞电学性能
Abstract
Cell surface coating refers to the process which encapsulate cell through the interaction between materials and functionalize the cell surface. This method has many biomedical applications, and also can be use in cell-based biosensors, thermal and chemical sensors, bio-mimicking sensors and other biological electronic devices. Among them, the cell electrode has an extremely wide range of applications. In order to research and design cell electrodes, we modified the surface of yeast cells by cell-encapsulation technology to enhance their electrical properties and try to make breakthroughs. Graphene has drawn wide attention due to its excellent electrical properties. Therefore,this paper attempts to coat the surface of yeast cells with the graphene sheets to enhance the conductivity of the cells. After modification of the yeast cell surface with aminophenylboronic acid, the graphene nanosheets reduced by chemical reduction can encapsulate the cell surface to form a conductive interface. The graphene nanosheets which is reduced by chemical reduction and deposited on the cell surface has good biocompatibility. So the coated cells are still capable of performing normal physiological activities and the coating process is less damage to the cells. At the same time, this paper also attempts to mix the graphene nanosheets reduced by chemical reduction with the gold nanoparticles to obtain the graphene nanosheets which carry the gold nanoparticles. Coated with this composite material, electrical performance of yeast cells can be more significantly enhanced.
Key Words:graphene;single cells encapsulation;hiberarchy;the electricity property of yeast cell
目 录
第1章 绪论 5
1.1 仿生学中的细胞表面工程 5
1.2 细胞包埋的历史 5
1.3 细胞包埋及其方法 6
1.3.1 层层自组装法 6
1.3.2 离子结合法 8
1.3.3 自形成法 9
1.4 细胞包埋的运用 10
1.4.1 细胞保护 10
1.4.2 细胞热稳定性提升 10
1.4.3 生物细胞治疗 11
1.4.4 细胞催化增强 11
1.5 课题的设计及研究意义 12
第2章 石墨烯分级结构在细胞表面的构建 13
2.1 前言 13
2.2 实验部分 14
2.2.1 实验方法 14
2.2.2 实验试剂、材料和仪器 15
2.3 结果与讨论 17
2.3.1 石墨烯的拉曼光谱表征 17
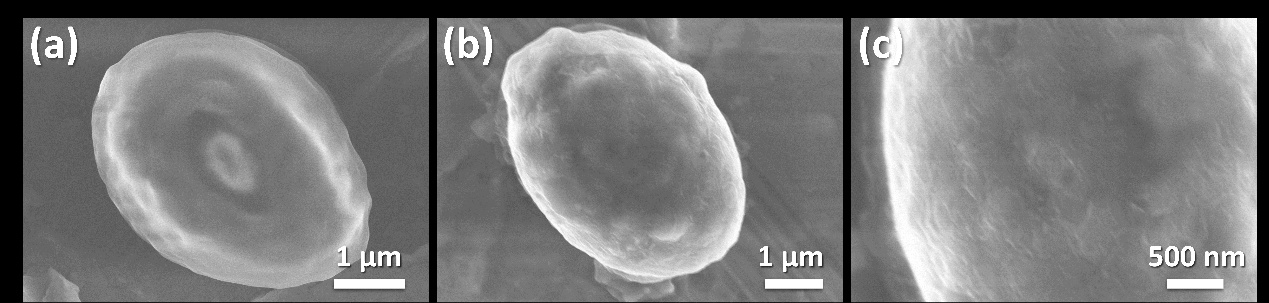
2.3.2 细胞形态表征 18
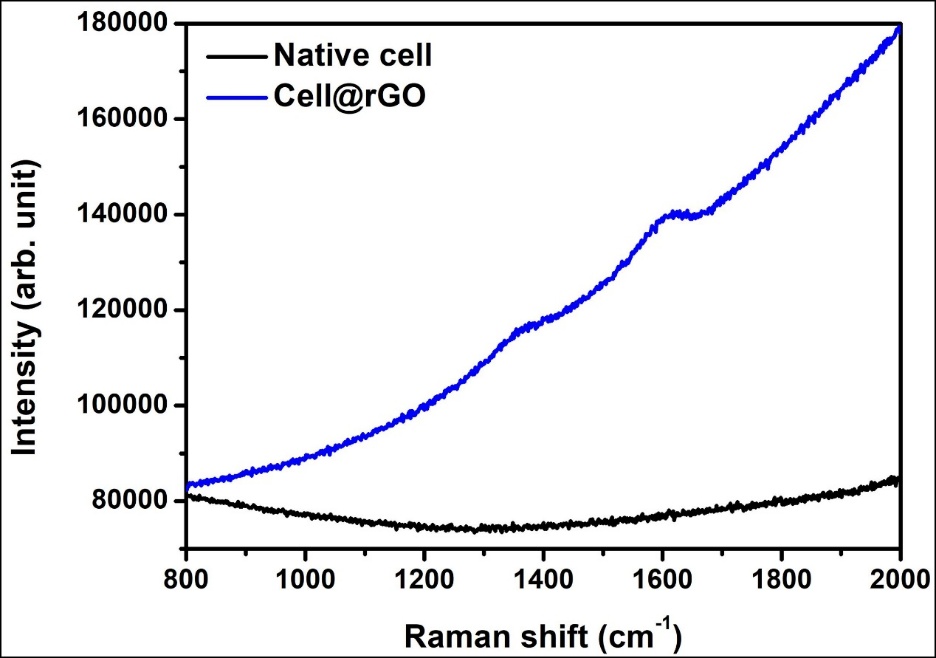
2.3.3 细胞拉曼图谱 19
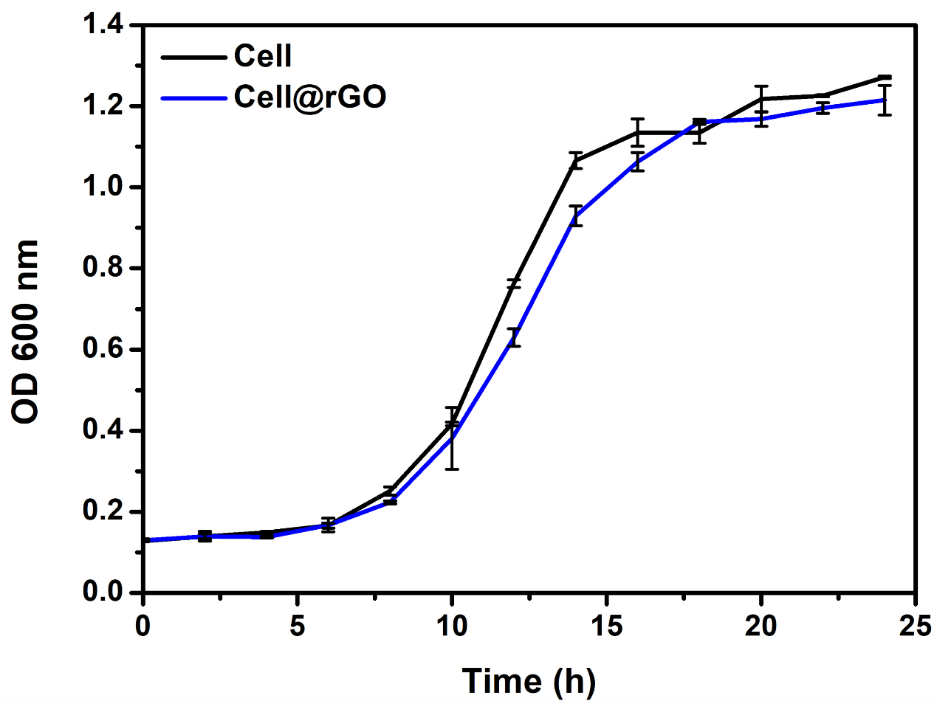
2.3.4 细胞生长曲线 20
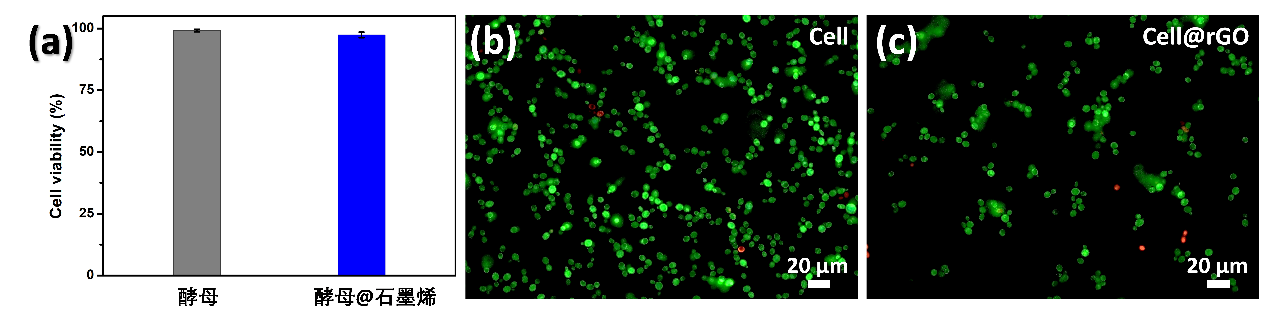
2.3.5 细胞活性测试 21
2.3.6 电学性能测试 21
2.3.7 担载纳米金颗粒后的包覆细胞的表征及性能测试 23
第3章 总结与展望 27
3.1 总结 27
3.2 展望 27
参考文献 28
致谢 33
第1章 绪论
仿生学的要素在于模仿自然生物的特性、生命活动等。[1]近几年有很多关于仿生学的工程设计以及生物医学的例子。然而,生物材料在生物医学的应用受到了生物自身免疫机制的影响,为了提高植入生物体内材料在生物体中的存活率,必须寻找合适的材料以适应生物免疫系统的自我识别过程。[2]而细胞表面工程学的研究基于对细胞表面进行修饰,可以有效的解决这一方面的问题。
1.1 仿生学中的细胞表面工程
近年来,涌现出了很多微型的生物电子设备,诸如生物细胞传感器、热化学传感器、仿生传感器及生物芯片技术等。[3-5]对于这些设备而言,特别是在一些条件苛刻的人工环境下,它们需要细胞长期的生存能力、功能性以及可持续性,在实际运用中,这些设备可能面临一些无机电极环境、光线直射下的干燥环境或者具有细胞毒性的基质环境。[2]在生物医学的应用往往需求哺乳类的细胞,这一细胞在实际运用中需要克服免疫力相关的问题,而对于电子生物应用而言,需要细胞在恶劣物理、化学环境下的长期的生存能力,因此常使用微生物细胞,细胞表面工程学可以对细胞表面进行修饰,给予细胞表面特殊的功能,合理地进行包覆,甚至能够起到保护细胞免受恶劣环境影响的作用。
细胞表面工程中的生物材料包括两种,一种为自然派生出的生物材料,另一种为模仿细胞膜的磷脂结构得到的自助装材料。[6-8]基于传统生物医学的工作方向,细胞包覆往往被应用于各种媒介中去,如细胞的出芽或者固定,设备的移植,伤口的修复以及组织工程等,但是对于细胞的保护却鲜有研究,特别是在一些环境严苛的生物电子设备的人工媒介中。[2]而对于这方面的研究,Fakhrullin,Paunov, Lvov, Choi和他们的合作者们在这一方面进行了讨论,并且在细胞表面各种成分的层层自助装上进行了很好回顾,Irina Drachuk , Maneesh K. Gupta , and Vladimir V. Tsukruk则就关于细胞表面工程对细胞进行强有力的保护例举了几个研究发现并进行了阐述。
1.2 细胞包埋的历史
通过利用细胞表面及包覆材料的静电交互作用已成功得到包覆好的具有生物相容性的功能化活性单个细胞。[9]在早期的工作中也研究了单细胞包埋后细胞的活性以及生长能力。[9]同时早期工作也证明了纳米尺度下的细胞包埋可以维持细胞的活性,控制细胞的分裂,保护细胞,以及使细胞表面功能化。[9]
在2000年,Möhwald发表了关于使用戊二醛固定人体红细胞并且在其表面通过层层自组装法包覆PSS纳米壳的文章。[10]在2002年,Lvov使用了牛血小板细胞作为一个小型的模板来实现单细胞包覆,他利用了聚合PDDA以及PSS的静电层层自组装在细胞表面进行包覆材料的沉积。[9]2003年,Mirkin发表了文章阐述在曲霉菌、青霉菌、毛霉菌以及链霉菌等的菌丝上单层自组装低核苷酸修饰的金纳米颗粒的方法。[11]在2006年,Tabrizian实现了大肠杆菌表面的纳米壳包覆。[12]在2009年,Tabrizian提出了一个模块化的方法来对非固定的人体血细胞进行包覆,即将血细胞沉积在二维基底上。[13]同时在2009年Fakhrullin发表了关于通过层层自组装法在细胞表面包覆掺杂了金或二氧化碳颗粒的壳层的文章。[14]
这些早期工作的发现,都为后续工作的进展以及单细胞包覆这一领域的发展提供了很好的研究方法
1.3 细胞包埋及其方法
在大部分细胞的包覆中,细胞表面工程使用的是自下而上自组装的超博且柔软的壳体进行包覆,在传统的处理方法中,常常面临着细胞活性的损失,免疫应激反应,营养物质及信号分子的传输限制以及空隙体积限制等重大挑战。[15]为了解决这些问题,常使用厚度为2 nm~100 nm的纳米片超博保护壳体,这些常用的壳体有着不同的形貌、不同的组成以及不同的分子间相互作用,它们的目的都是给细胞与外界物质交换提供更好地传输通道,给与细胞更好的机械性能,使细胞表面功能化以及在恶劣环境中保护细胞。
厚度低于100 nm的超薄材料单细胞包埋的研究历史很短,最早的相关研究是在2000年对于单个的红细胞或者细菌作为独立的研究对象进行相关的化学处理。[9]
在过去十年里,单细胞纳米包埋这一领域有了大步的发展,并且对许多科技领域有突出的贡献,例如细胞治疗、细胞传感器、生物催化以及单细胞生物学的基础研究。基于不同的目的或者不同的细胞特性,许多哺乳类或者微生物细胞都利用不同材料进行了纳米尺度上的包覆,并且发展了许多相关的包覆方法。[9]细胞纳米包埋不仅仅是传统意义上的对多个细胞进行微观包覆(如对胰岛细胞群进行水凝胶的多细胞包埋),同时也可以是在不影响细胞活性的前提下在单细胞水准上的包覆。[16-19]细胞纳米包埋包含了生物物理学,化学,材料科学与工程,生物学,生物医学工程学以及环境科学等学科领域。[9]
1.3.1 层层自组装法
层层自组装法在2008年首先被提出用于提升酵母的矿化能力并渐渐成为一种常规的有机体的修饰方法。[19]层层法是一种用于形成薄膜的技术,它通过交替沉积带有相反电荷的材料或者具有交互作用力的材料来修饰有机体。[20]酵母细胞壁的化学组成为带有弱电负性的多糖体,甘露糖,N-乙酰化葡萄糖氨等,同时含有少量的与矿化相关残基或者官能团。[21]多聚氯化二甲基己二烯铵是一种电正性的聚合物并且它的官能团可以吸附在电负性的酵母细胞表面上从而形成一个电正性的表面包覆层。接下来,加入带有相反电荷的聚丙烯酸分子并且它们也会吸附在多聚氯化二甲基己二烯铵上以形成电负性的包覆层。通过几个周期的交替形成两种聚合物,就可以在酵母细胞表面上形成含有丰富的功能化残基的薄膜并且细胞表面的矿化能力也有显著的提升。[19,22]对于钙矿化,富含羧酸盐基团的聚丙烯酸可以与钙离子相互作用,因此也是最外层的包覆层。因为有着丰富的聚丙烯酸,钙离子更易于集中在细胞表面周围并且引发细胞表面的磷酸钙的沉积(图 1.1a),进而可以得到核壳结构的磷酸钙酵母混合物。因此,层层法处理使得酵母细胞从非矿化细胞转变为矿化细胞。
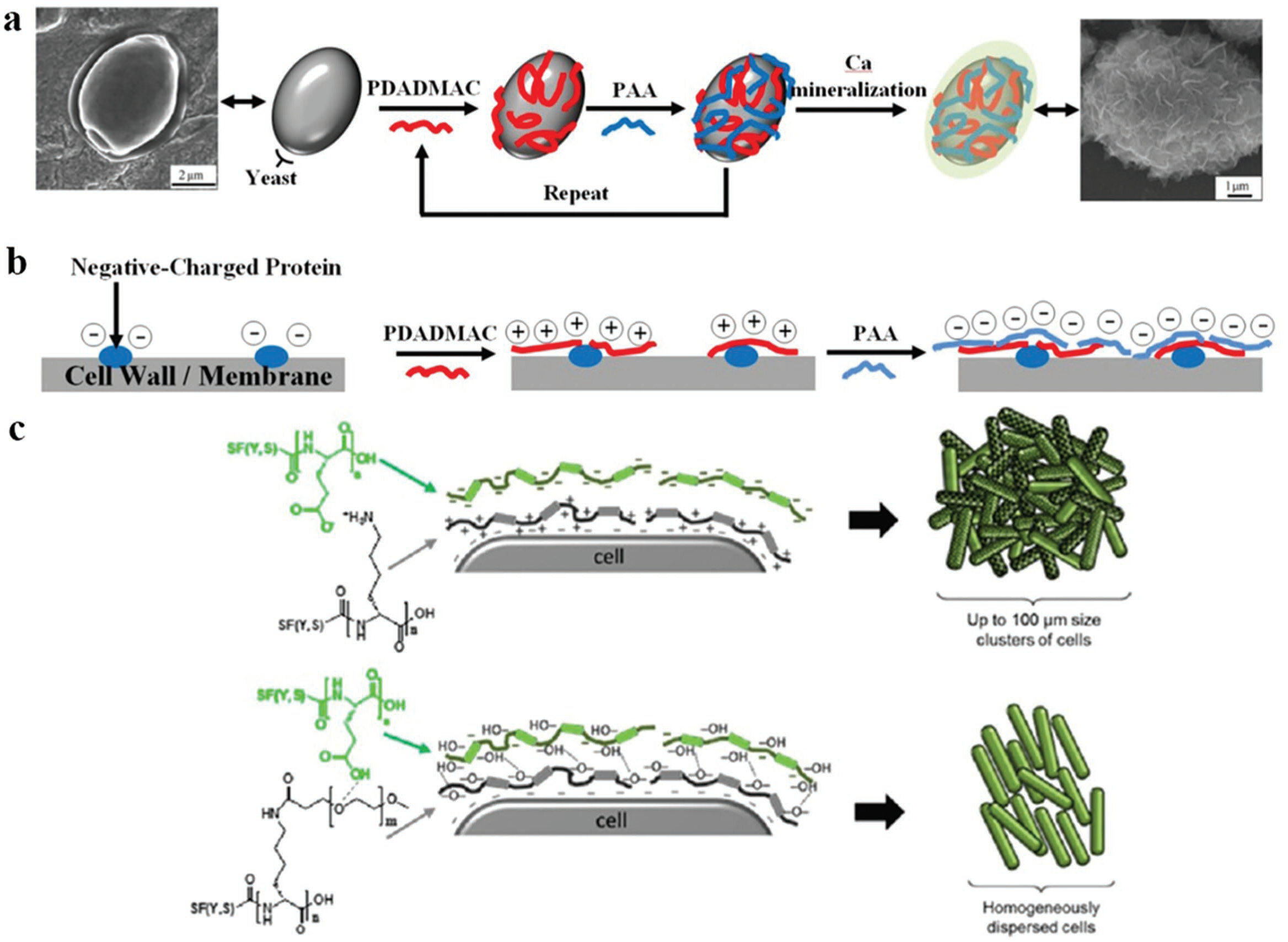
图1.1 细胞的层层法修饰:a) 酵母细胞表面人工构筑磷酸钙壳体;b) 通过层层法增加结合位点或者表面电子密度;c) 细胞在不同丝状共聚物的层层包覆法下的聚合[25]
层层法是一种有效的细胞表面修饰方法。[23]在组装的薄膜里,聚合物分子就像分支一样,不仅仅连接位于下方的带有相反电荷的聚合物,也增加了外层包覆层的电子位点或功能化官能团(图 1.1b)。[24]相应地,也可以通过控制层层法的周期重复次数来调节残基密度和随后的矿化程度,并且最终可以用于控制随后在细胞表面矿化壳体的密度以及厚度。此外,部分聚合物 也可以像桥梁一样连接各个细胞,并且引导以及控制细胞在溶液中聚合(图 1.1c)。[25]
1.3.2 离子结合法
在另一些情况下,细胞表面与矿质离子之间强的电子相互作用可以直接形成细胞与材料的复合。钙离子在几乎所有的有机生物体中都是必不可少的,尤其是钙离子在细胞生理活动中作为第二信号分子。[26]非特异性免疫的效应细胞可以通过细胞膜上的离子受体从溶液中占据钙离子。[27]因此,这些钙离子受体可以作为钙离子矿化的成核位点以及离子结合位点。由于其正二价的特点,钙离子也可以作为连接两个电负性分子的桥梁。根据离子结合特点,与柠檬酸盐修饰的金纳米颗粒混合的氯化钙溶液可以引发金在酵母细胞壁表面的聚合以形成一个金壳。[28]随着这个思路进行,混合还原氧化石墨烯及钙-金纳米颗粒可以在酵母细胞上产生还原氧化石墨烯壳体(图 1.2a),而且细胞与材料的识别与相互作用是由于钙离子结合在细胞表面上而产生的。[29]
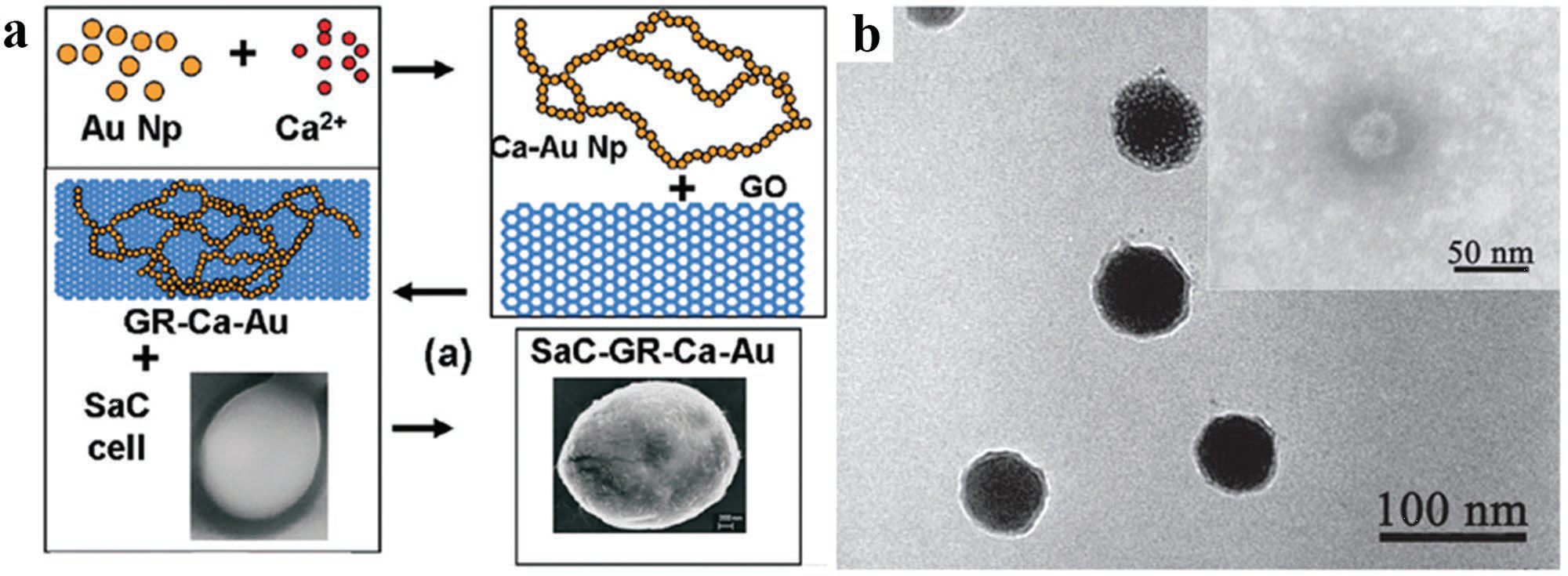
图1.2 离子结合法修饰:a) 使用钙离子功能化的金纳米颗粒被转变为分支链进行组装,随后,钙-金纳米颗粒沉积在氧化石墨烯片层上以形成氧化石墨烯-钙-金组装体系并还原形成还原氧化石墨烯-钙-金组装体系,并随后利用功能化的离子在酵母细胞表面形成交互界面[29];b) 日本脑炎疫苗颗粒由于其表面高的电负性可以在富含钙离子的条件下直接矿化[31]
此外,许多病毒颗粒的表面有很高的电负性。[30]它们可以直接吸附高密度的阳离子并且引起局部的正电荷过饱和,从而引发此处产生材料壳体。以日本脑炎疫苗为例,它可以在富含钙离子的生物培养中吸附大量作为阳离子的钙离子并引起钙离子矿化(图 1.2b)。[31]通过直接引入细胞表面成核位点的非均相成核也是一个产生材料壳体的方法,例如,预吸附在杆菌细胞上的铂纳米颗粒可以引起电磁性的钴镍铂壳体在细胞周围形成。[32]
不同于上述提及的层层法试图在有机体表面进行修饰,尤其是对于病毒颗粒等表面具有高电负性的生物体,离子结合法更易于材料壳体的形成。然而,这一方法不适用于常规的生物体体,因为它要求生物体表面有着相当高密度的离子受体或者电子电荷。
1.3.3 自形成法
不同于酵母细胞,哺乳类细胞没有细胞壁结构并且它们对于任何材料处理都很敏感。直至现在,对哺乳类细胞利用材料壳体进行有效的包覆都仍是一个挑战。一个折中的修饰方法为通过使用足量的聚电解质来修饰细胞表面从而简化层层法修饰为单层修饰。最近,Choi的团队展示了人子宫颈癌传代细胞通过聚合物辅助而进行的硅化作用。[33]细胞与作为阳离子的乙烯亚胺分子(一种硅化作用的催化模板)在溶液中混合,之后加入硅化前体以引发二氧化硅壳层的形成。在人子宫颈癌传代细胞上的二氧化硅的成功形成归因于乙烯亚胺高的正电荷密度,但是这一聚合物具有细胞毒性。[34]尽管壳体壳体最终生成,这一包覆细胞的存活时间仅仅维持在12小时。因此,对于改善这一方法最重要的问题是寻找对哺乳类细胞具有细胞相容性的合适的聚电解质。
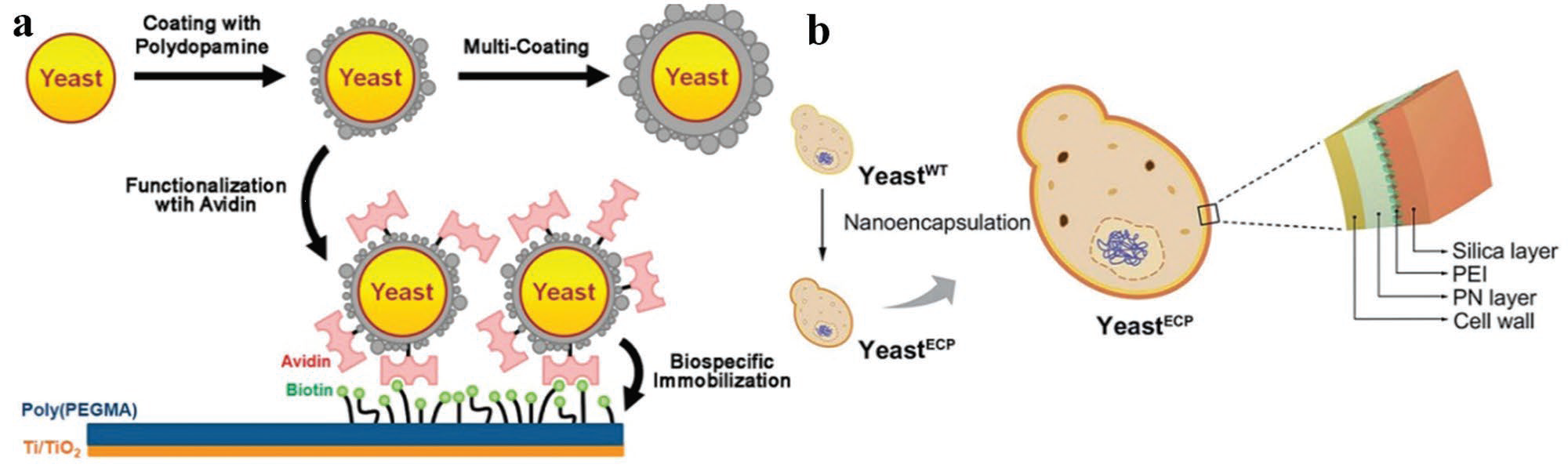
图1.3 自形成法修饰:a) 单个细胞的聚多巴胺包覆及人工壳体的功能化示意图[36];b) 由有机的聚去甲肾上腺素和无机的二氧化硅包覆层组成的人工壳体[37]
自聚合是另一种改善生物体矿化能力并形成壳体的方法。启发自贻贝类粘附蛋白的聚多巴胺是一种可靠的在包括生物体表面在内的各种基底上引入功能化矿化基团的药剂。[35]修饰常在具有基本条件的多巴胺溶液中进行。尽管确切机制并不清楚,可以推测的是聚多巴胺与基底通过领苯二酚及胺类基团形成了高强度的共价键及非共价键交互作用力。沿着这一思路。可以在酵母表面包覆一层聚多巴胺壳体。(图 1.3a)。[36]另外,聚多巴胺与表面修饰的胺类及硫醇类官能团的化学反应是可行的,如其与抗生物素蛋白的功能化。[36]按照这种自聚合,具有额外羟基的多巴胺衍生物聚去甲肾上腺素由于其优异的细胞相容性有着更好地包覆效果。聚去甲肾上腺素壳层也可以用于嫁接聚乙烯亚胺,使得能在不损伤细胞活性的同时在酵母细胞上进行硅化(图 1.3b)。[37]实际上,聚多巴胺已成功用于化学修饰与其他哺乳类细胞具有相似细胞膜的红血球。[38]因此,在聚多巴胺或者聚去甲肾上腺素上吸附聚乙烯亚胺来修饰的哺乳类细胞对于之后的硅化处理比直接进行聚乙烯亚胺的吸附有着更好地细胞相容性。
1.4 细胞包埋的运用
以上是毕业论文大纲或资料介绍,该课题完整毕业论文、开题报告、任务书、程序设计、图纸设计等资料请添加微信获取,微信号:bysjorg。
相关图片展示:

课题毕业论文、开题报告、任务书、外文翻译、程序设计、图纸设计等资料可联系客服协助查找。



