由二维材料嵌层制备的MC复合材料及在电催化中的应用毕业论文
2020-04-05 11:01:10
摘 要
在非贵金属催化剂中,金属有机框架(MOFs)基材料得到广泛关注。金属/金属化合物与MOFs衍生碳复合形成的催化剂成为研究热点。本文提出一种在叶片状沸石咪唑酯骨架结构材料(ZIF-L)表面直接生长氢氧化钴纳米片(Co(OH)2 nanosheets),构筑出Co(OH)2与ZIF-L嵌层复合物。通过高温煅烧该复合物得到CoNC催化剂,并将其用于析氧反应(OER)和氧还原反应(ORR),展现出较好的催化性能,且具有较优的稳定性。对于OER,CoNC500在10 mA cm-2电流密度处的电极电位为1.61 V,即过电位为380 mV。对于ORR,CoNC500具有较高的半波电位——0.827 V。通过进一步地改变ZIF-L的加入量,得到ZIF-L的加入量对其OER催化性能的影响关系。本文的工作对在MOFs类材料表面直接生长金属氧化物/氢氧化物提供了很好的实例,对广泛地在不同类型MOFs上合成其他金属氧化物/氢氧化物具有指导意义;同时,对今后调控该类催化剂的催化性能具有借鉴意义。
关键词:沸石咪唑酯骨架结构材料;氢氧化钴纳米片;CoNC;电化学析氧反应;氧气还原反应
Abstract
Metal organic frameworks (MOFs) attract much attention among non-precious catalysts in recent years. Numbers of researchers pay attention on the composite catalysts consisted of metal/metal compound and MOFs derived carbon and their application. In this paper, we report a strategy to make metal hydroxide growing on leaf-like zeolitic imidazolate frameworks (ZIF-L) directly. As a result, we obtained Co(OH)2 nano-sheets/ZIF-L embedded layer composite. After pyrolysis, the CoOx loaded on nitrogen doped carbon (CoNC) catalysts was synthesized successfully. The CoNC500 was used as catalysts for oxygen evolution reaction (OER) and oxygen reduction reaction (ORR). The obtained CoNC500 catalysts exhibits excellent OER activity with 380 mV over-potential at the current density of 10 mA cm-2 and ORR activity with half-wave potential of 0.827 V. Furtherly, we regulate the adding concentration of ZIF-L to figure out the relationship between the catalytic activity and the concentration of ZIF-L. With the decreasing concentration of ZIF-L, the catalytic activity of CoNC decreases. Overall, we provide a sample of metal (hydr)oxide growing on MOFs derictly and represent its OER and ORR catalytic activity, which can be extended to other similar synthesis of metal (hydr)oxide/MOFs.
Key Words:ZIF-L; Co(OH)2 nano-sheets; CoNC; OER; ORR
目 录
摘 要 I
Abstract II
第1章 绪论 1
1.1前沿 1
1.2质子交换膜燃料电池阴极的电化学反应 1
1.2.1质子交换膜燃料电池简介 1
1.2.2阴极氧化还原反应 3
1.3 电解水反应的电化学反应 5
1.3.1电解水析氧反应简介 5
1.4MOF及其复合材料衍生的金属/碳材料在电化学反应中的应用 5
1.4.1过渡金属/碳体系材料的发展 5
1.4.2金属/碳体系材料作为燃料电池阴极催化剂的研究进展 6
1.4.3金属/碳体系材料作为电解水催化剂的研究进展 6
1.4.4 MOFs及其复合材料衍生的金属/碳材料的研究进展 7
1.5本论文的研究目的、内容及意义 9
第2章 实验材料与研究方法 11
2.1实验试剂与仪器 11
2.2催化剂测试以及表征方法 12
2.2.1结构、形貌、成分分析 12
2.3催化剂的电化学性能表征 12
2.3.1电极浆料制备和电极制备 12
2.3.2催化剂的ORR催化性能表征 13
2.3.3催化剂的ORR转移电子数计算 13
2.3.4催化剂的OER性能测试 13
2.3.5催化剂的OER性能稳定性测试 13
第3章 二维Co(OH)2纳米片与二维ZIF-L复合衍生CoNC材料及其OER,ORR性能 14
3.1前言 14
3.2 实验方法 15
3.2.1 Co-N-C催化剂制备 15
3.2.2 电极的制备 15
3.3 结果与讨论 16
第4章 结论与展望 23
参考文献 24
本科期间发表论文 29
本科器件参与的项目与基金 29
致谢 29
第1章 绪论
1.1前沿
目前,化石燃料以飞快的速度被消耗加之生态环境面临着越来越严重的破坏。诸多严峻的环境问题使人们意识到发展清洁能源的重要性,同时也加快了人类社会发展清洁能源的步伐。因此,探索和开发新型能源以及储能器件成为工业界和科研人员广泛关注的课题[1]。
在能源方面,氢能被认为是21世纪最理想的、最具有应用前途的绿色能源[2]。但是,利用绿色手段大规模商业化制备高纯度的氢气成为阻碍氢能源大规模使用的一个研究难点。因此,如何采用绿色的手段大规模合成很高纯度的氢气引起研究者们的研究兴趣。就目前的工业界而言,广泛用来制备氢气的方法仍然是利用化石燃料制备氢气。尽管利用化石燃料制备氢气是主流的方法,但是其步骤繁琐,氢气纯度低,环境不友好等问题要求人们迫切发展更加绿色、高效的制备氢气的方法。作为未来最有前途的,最可行的利用绿色方法制备高纯度氢气的方法——电解水制氢,因过高的生产成本而不能大规模商业化使用。其主要的两大难题是电解水反应的析氧、析氢反应的高过电位导致的高耗能和电解水使用的贵金属催化剂的巨额成本。
与此同时,以氢气为燃料的质子交换膜燃料电池由于具有效率高、绿色环保和可靠性高等特点,自上个世纪就已经得到人们的关注和研究。但是,质子交换膜燃料电池中昂贵的铂碳催化剂、较大的氧还原反应过电位等问题使得其商业化的步伐受阻[3, 4]。
因此,发展新型的、高效的、低价的电化学催化剂材料解决上述电化学问题对人们认识和发展新型清洁能源和储能器件,以及对整个社会的可持续发展具有重要意义[2]。
1.2质子交换膜燃料电池阴极的电化学反应
1.2.1质子交换膜燃料电池简介
燃料电池(fuel cell, FC)是上世纪人们开发的一种发电装置,相较于传统电源具有很好的环境友好性,和非常高的能量转换效率。其基本的工作原理是通过催化反应将燃料和氧气发生反应,将化学能转变电能[5]。迄今为止,燃料电池得到非常快速的发展。按照电解质分类,燃料电池具有多种类型:固体氧化物燃料电池(Solid Oxide Fuel Cell, SOFC)、碱性燃料电池(Alkaline Fuel Cell, AFC)、磷酸燃料电池(Phosphoric Acid Fuel Cell, PAFC)、熔融碳酸盐燃料电池(Molten Carbonate Fuel Cell, MCFC)和质子交换膜燃料电池(Proton Exchange Membrane Fuel Cell, PEMFC)[6, 7]。其中,质子交换膜燃料电池因其工作温度低、比功率高等优势最具有发展前景,并成功作为动力电源得到初步商业化[6]。
质子交换膜燃料电池单电池主要工作器件是阳极、质子交换膜和阴极[6]。其在酸性介质中的工作原理如图1.1所示:
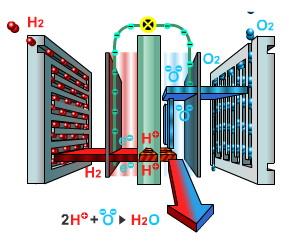
图1.1 质子交换膜燃料电池工作原理图
Figure 1.1Working scheme of PEMFCs
氢气(H2)从外界经过流场板中的流道与阳极催化剂接触发生氧化反应,同时生成氢离子(H )并释放一个电子;H 经过质子交换膜(Proton Exchange Membrane, PEM)后到达阴极,电子由外电路到达阴极;氧气(O2)从流道进入阴极,在催化剂的作用下得到H 和电子,进行氧气还原反应[8]。
氢氧化反应式:H2→2H 2e- E0=0 V (vs. RHE) (1-1)
氧还原反应式:1/2O2 2e- 2H →H2O E0=1.229 V (vs. RHE) (1-2)
总反应式:H2 1/2O2→H2O E0=1.229 V (vs. RHE) (1-3)
尽管二十世纪六十年代,美国已经将PEMFC成功应用于航空领域,但PEMFC的发展却没有十分迅速。上世纪八十年代,PEMFC作为汽车动力能源再次得到世界各国的广泛关注,并得到迅速发展上世纪九十年代,国内掀起了PEMFC的研究热潮。以武汉理工大学、清华大学、同济大学和中国科学院大连化学物理研究所为代表的研究单位对PEMFC的研究做出了重要贡献,并相继研制出武汉理工大学“楚天”号燃料电池汽车、清华大学“清能”号燃料电池大巴、同济大学“超越”号燃料电池汽车等。直至今日,PEMFC的商业化进程仍然有很大的难题,其原因有以下几点:(1)高昂的材料价格限制了其大规模商业化[9, 10]。众所周知,PEMFC中阳极和阴极的催化剂为铂碳(Pt/C)。贵金属铂的价格十分高昂。同时,PEMFC中的其他材料,例如质子交换膜为全氟磺酸膜(Nafion),其价格也十分高昂[11, 12]。(2)传统Pt/C催化剂的在运行过程中的不稳定性限制了其寿命和性能。一方面,氢气中的少量杂质(CO等)会使Pt/C催化剂的性能降低甚至失去活性。另外,燃料电池运行过程中发生的Ostwald熟化[13, 14]导致铂纳米颗粒(Pt nanoparticle)团聚,晶粒变大,活性位点变少,催化剂活性因此降低[15]。(3)其他工程问题,例如水管理,温度调控等[6, 7]。
1.2.2阴极氧化还原反应
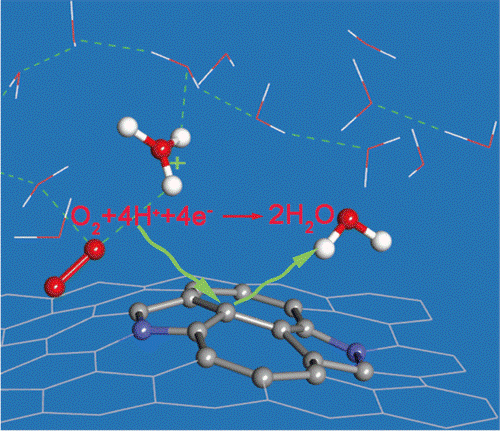 燃料电池的阴极的氧化还原反应由于较慢的反应动力学(比阳极小5个数量级)因而需要更多载量的Pt/C催化剂,一直备受关注[4, 10]。此外,相较于两电子的氢气氧化反应(HOR),氧气还原反应(ORR)是一个四电子反应,反应过程更为复杂[8, 9, 13]。
燃料电池的阴极的氧化还原反应由于较慢的反应动力学(比阳极小5个数量级)因而需要更多载量的Pt/C催化剂,一直备受关注[4, 10]。此外,相较于两电子的氢气氧化反应(HOR),氧气还原反应(ORR)是一个四电子反应,反应过程更为复杂[8, 9, 13]。
图1.2 ORR反应示意图[16]
Figure 1.2 Scheme of ORR mechanism[16]
如公式1-2所示,其理论标准电压为1.229 V,但是其反应过程较为复杂,伴随着二电子反应生成双氧水以及反应过程中具有多种中间产物,导致能垒的存在,并直接导致ORR具有较大的过电位。即使是性能最好的Pt/C催化剂,其过电位也仍有300 mV及以上[9, 17]。一般而言,Pt/C催化剂在酸性溶液或碱性溶液中发生氧化还原反应是以四电子反应路径进行[17]。但是,非铂类催化剂在反应过程中往往不能实现四电子反应,过程中伴随着副产物的产生,例如双氧水。因此,研究者们希望在开发的非贵金属基催化剂能够催化四电子反应,并且尽量避免副产物的产生。
碱性条件下的四电子和二电子反应式[8, 10]:
O2 H2O 4e-→4OH- (1-4)
O2 H2O 2e-→OOH- OH- (1-5)
OOH- H2O 2e-→3OH- (1-6)
酸性条件下的四电子和二电子反应式[8, 10]:
O2 4H 4e-→2H2O (1-7)
O2 2H 2e-→H2O2 (1-8)
H2O2 2H 2e-→2H2O (1-9)
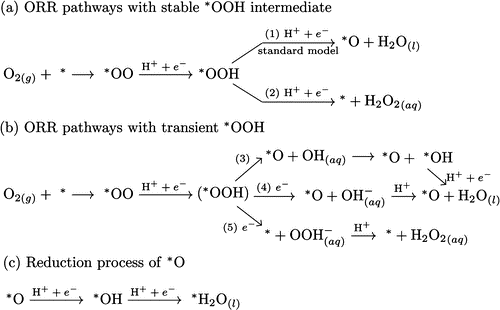 实际研究中,ORR过程的中间体难以通过实验直接检测,研究人员通过密度泛函理论(Density functional theory, DFT)计算[18, 19],得到一些可能的反应路径。O2分子被吸附到催化剂表面形成吸附氧分子*O2,在不同的反应路径中,*O2会转变为不同的中间体,例如*OOH、*O、*OH、*HOOH等[20, 21]。在酸性条件下,一般对于金属催化剂,得到广泛认同的反应路径有三种:解离路径、缔合路径和过氧化路径。对于适用于解离的反应路径而言,*O2的氧氧键(O-O)会首先发生断裂,形成*O中间体;紧接着,*O依次得到H ,前后分别形成*OH和*H2O。对于缔合路径,*O2得到H 首先形成*OOH中间体,随后O-O断裂,生成*O和*OH。解离路径适用于金属催化剂表面氧覆盖度较低的情况而缔合路径适用于覆盖度较高的情况。过氧化路径即是*O2中间体在O-O断裂之前就形成*HOOH。但是,值得注意的是,针对某种具体的材料,应按照实际情况计算分析反应路径以及中间体。
实际研究中,ORR过程的中间体难以通过实验直接检测,研究人员通过密度泛函理论(Density functional theory, DFT)计算[18, 19],得到一些可能的反应路径。O2分子被吸附到催化剂表面形成吸附氧分子*O2,在不同的反应路径中,*O2会转变为不同的中间体,例如*OOH、*O、*OH、*HOOH等[20, 21]。在酸性条件下,一般对于金属催化剂,得到广泛认同的反应路径有三种:解离路径、缔合路径和过氧化路径。对于适用于解离的反应路径而言,*O2的氧氧键(O-O)会首先发生断裂,形成*O中间体;紧接着,*O依次得到H ,前后分别形成*OH和*H2O。对于缔合路径,*O2得到H 首先形成*OOH中间体,随后O-O断裂,生成*O和*OH。解离路径适用于金属催化剂表面氧覆盖度较低的情况而缔合路径适用于覆盖度较高的情况。过氧化路径即是*O2中间体在O-O断裂之前就形成*HOOH。但是,值得注意的是,针对某种具体的材料,应按照实际情况计算分析反应路径以及中间体。
图1.3 酸性介质中ORR反应三种可能的路径[22]
Figure 1.3 Three possible ORR pathways in acid solutions[22]
1.3 电解水反应的电化学反应
电解水制备氢气因其工艺简单、绿色环保、产品纯度高等技术特点成为当下世界各国研究者关注的热点。但是,如何降低电解水的阴极析氢反应的过电位是电解水制氢实现大规模工业化的关键。因此,开发具有低成本、长寿命、低过电位的催化剂成为重中之重[23]。
1.3.1电解水析氧反应简介
尽管电解水制氢的应用前景乐观。然而,其催化效率受到阳极——析氧反应(Oxygen Evolution Reaction, OER)反应动力学的限制[24]。OER是一个复杂的过程,包括固体催化剂、电解质、气相和液相反应物以及产物的相互作用[25]。在碱性介质中的OER反应式如下:
4OH-→2H2O O2 4e- (1-18)
OH-失去电子被氧化为H2O和O2。其在酸性介质中的反应式如下:
2H2O→O2 4H 4e- (1-19)
H2O失去电子被氧化为和O2[25]。由于析氧反应过程动力学很缓慢,因故成为了电解水制氢的控制反应。当下,对于非贵金属基的OER催化剂而言,在10 mA cm-2的电流密度处,需要极大的过电位。很多贵金属或非贵金属催化剂在碱性电解质中能够表现出高活性和稳定性。但是,在酸性介质中,仅有氧化铱(IrOx)和氧化钌(RuOx)可以在较低的过电位下实现较高的电流密度[26]。
传统的OER贵金属催化剂(例如RuOx、IrOx)的昂贵的价格限制了电解水进一步大规模推广。因此,开发高效的,具备低过电位的,稳定性好的廉价OER催化剂成为研究者关注的重点[2, 10, 20]。
以上是毕业论文大纲或资料介绍,该课题完整毕业论文、开题报告、任务书、程序设计、图纸设计等资料请添加微信获取,微信号:bysjorg。
相关图片展示:

课题毕业论文、开题报告、任务书、外文翻译、程序设计、图纸设计等资料可联系客服协助查找。



