四氧化三铁纳米粒子的拟酶活性及其与植物酶的复合作用毕业论文
2020-04-08 13:25:34
摘 要
纳米材料特殊的性质使其在世界范围内引起研究热潮,纳米颗粒对植物生长影响的也被深入研究,但是对于纳米粒子与植物内酶的复合作用机理尚不明确。本研究的目的是探究三种纳米氧化铁的过氧化物模拟酶活性以及其与多种植物过氧化物酶相互之间作用的具体方式,通过纳米氧化铁与植物中辣根过氧化物酶的正交复合,在过氧化氢(H2O2)存在下,与3,3,5,5-四甲基联苯胺(TMB)反应,测量底物反应速度,比较二者复合效果与其单独反应效果的优劣。
结果表明,三种纳米氧化铁均具有过氧化物模拟酶活性,并且在相同纳米氧化铁浓度时,模拟酶活性呈现出Fe3O4 MNPs>γ-Fe2O3 NPs>α-Fe2O3 NPs。在相同植物过氧化物酶浓度时,酶活性菠菜>甜瓜>拟南芥>小白菜。当纳米氧化铁与植物过氧化物酶复合反应时,二者会相互抑制酶活性,且浓度越高抑制效果更明显。但仍然能够促进底物的反应,并且比单独使用一种酶的活性更强。这表明了纳米氧化铁在植物保护和生长调节剂方面有独特的优势和广阔的应用前景。
关键词:纳米氧化铁;过氧化物酶;植物
Abstract
The special nature of nanomaterials has caused a worldwide upsurge of research, and the effects of nanoparticles on plant growth have also been studied in depth. However,the mechanism of the interaction between nanoparticle and plant enzymes is not yet clear.The purpose of this study was to explore the specificity of the interaction between three nanoscale ferric oxide peroxidases and their interaction with various plant peroxidases.Through the orthogonal compounding of nano iron oxide and horseradish peroxidase in plant,in the presence of H2O2,reacting with TMB to measure the substrate reaction rate,and comparing the composite effect of the two and the advantages and disadvantages of the separate reaction effect.
The results show that all three kinds of nano iron oxides have the activity of simulated enzyme,and at the same nanometer iron oxide concentration,the simulated enzyme activity Fe3O4 MNPsgt;γ-Fe2O3 NPsgt;α-Fe2O3 NPs.At the same plant peroxidase concentration,enzyme activity was spinachgt; melongt; Arabidopsis thalianagt;pakchoi.When nano-iron oxide reacts with plant peroxidase,both of them inhibit each other's enzyme activity,and the higher the concentration is,the more effective the inhibitory effect is.However,it still promotes the reaction speed of the substrate and is more active than a single enzyme. This shows that nano-iron oxide has unique advantages and broad application prospects in plant protection and growth regulators.
Key words: Nano iron oxide; Peroxidase; Plant
目录
摘要 I
Abstract II
第1章绪论 1
1.1 研究背景及意义 1
1.1.1 纳米氧化铁 1
1.1.2 过氧化物酶 2
1.2 研究目的与内容 3
1.2.1课题的提出 3
1.2.2研究的目的 3
1.2.3研究的内容 3
第2章实验材料和方法 4
2.1实验设备和试剂 4
2.1.1 实验设备 4
2.1.2实验试剂 4
2.2 实验材料 5
2.3实验测定 5
2.3.1 纳米氧化铁的表征 5
2.3.2过氧化物酶(POD)活性的测定 6
第3章 结果与分析 8
3.1 不同种类纳米氧化铁的过氧化物模拟酶活性比较 8
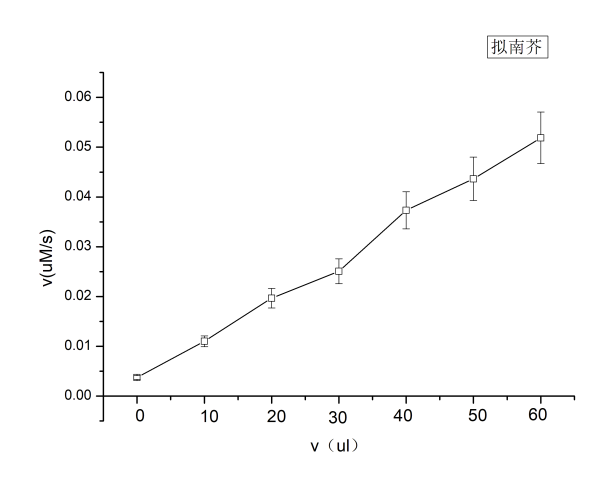
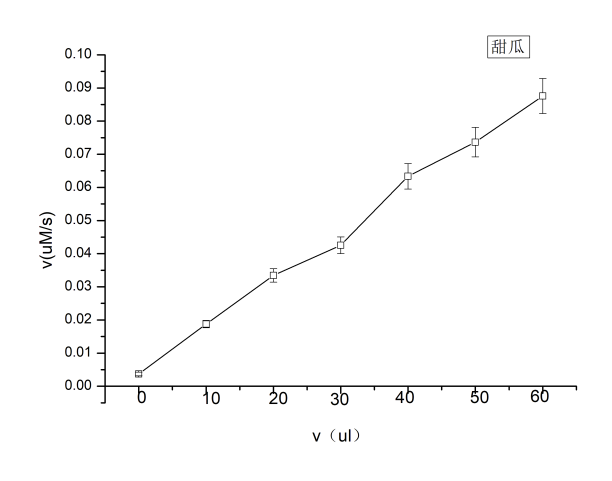
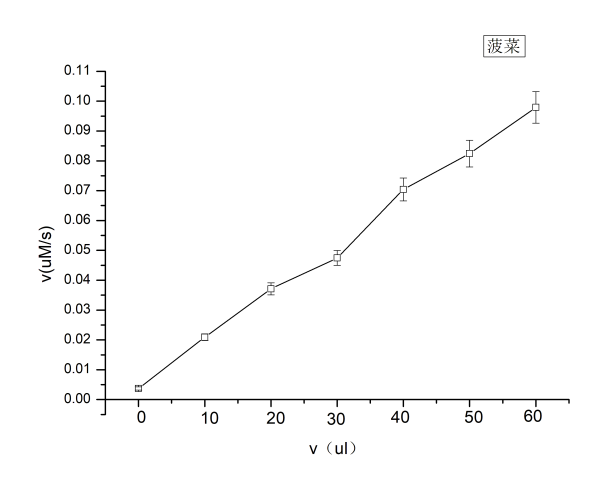
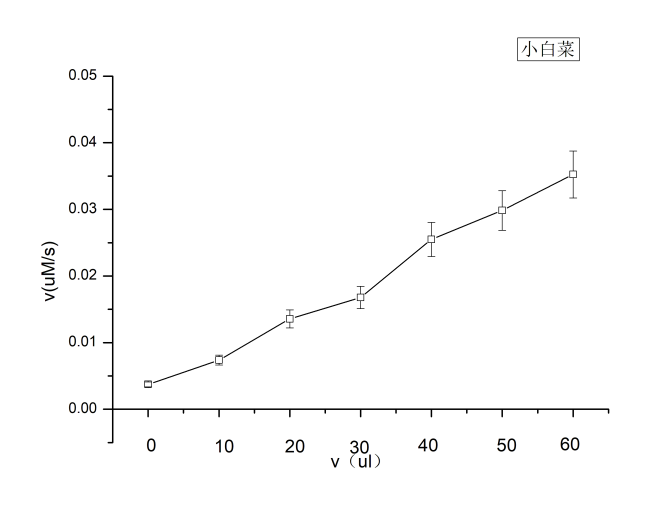
3.2不同种类植物过氧化物酶活性比较 9
3.3 纳米氧化铁与植物过氧化物酶的正交实验 10
3.3.1 Fe3O4 MNPs与植物过氧化物酶的正交实验 10
3.3.2 α-Fe2O3 NPs与植物过氧化物酶的正交实验 12
3.3.3 γ-Fe2O3 NPs与植物过氧化物酶的正交实验 13
3.3.4拟南芥过氧化物酶与纳米氧化铁的正交实验 15
3.3.5甜瓜过氧化物酶与纳米氧化铁的正交实验 16
3.3.6 菠菜过氧化物酶与纳米氧化铁的正交实验 18
3.3.7 小白菜过氧化物酶与纳米氧化铁的正交实验 19
第4章结论 21
参考文献 22
致谢 25
第1章绪论
1.1 研究背景及意义
1.1.1 纳米氧化铁
纳米材料特殊的性质使其在世界范围内引起研究热潮,例如纳米颗粒对植物生长影响的研究。但是对于纳米粒子与植物内酶的复合作用机理尚不明确。基于本实验室关于不同种类纳米氧化铁对西瓜影响的研究[1],更深入的探究四氧化三铁纳米粒子(Fe3O4 MNPs)与植物内酶的复合作用。
纳米粒子相比其他类型的材料具有许多优越的性能。如高矫顽力、超顺磁性、高磁化率、低居里温度[7]等,磁纳米粒子引起了很多学科研究者的兴趣,包括数据存储、磁流体、生物应用和催化等方面。特别是数据存储和铁磁的应用研究,导致目前在许多商业上都开始应用磁性纳米粒子。目前,磁性纳米粒子还能用于重要的生物应用领域,包括生物实体检测(核酸、蛋白质、酶、病毒、细菌、细胞)等和磁分离、临床诊断和治疗(如核磁共振)、靶向药物及生物标记等。其中磁性氧化铁纳米粒子有可能应用在体外诊断,并且它也是器件具有可调的化学和物理性能的关键和选择建筑的纳米结构材料[8]。
Fe3O4 MNPs的小尺寸(从1到100 nm)和大表面积决定了Fe3O4 MNPs的特定物理化学性质,这些特性与各自宏观形式的性质不同[9][10]。例如,由于能量过量,小于10nm的MNPs反应性高;尺寸约为1 nm的MNPs往往会与其他化学物质发生聚集和反应[11]。还发现活性植物组织中过量的磁性NPs会导致氧化应激并抑制光合作用[12]。
1.1.2 过氧化物酶
过氧化物酶一般由植物或真菌分泌一类重要的细胞体外酶。它们具有较高的氧化还原电位,广谱的底物范围,能够降解多种污染物。它们在污染治理、环境修复上有独特的优势和广阔的应用前景。近年来,过氧化物酶在处理含酚废水和印染废水脱色中的应用已经得到广泛的关注和深入研究。与传统方法相比,用过氧化物酶处理有机废水,尤其是含有酚或苯胺类化合物的有机废水,具有适用范围广,高效经济的优势。跟一般的生化处理不同,细胞体外酶不受底物和介质生物毒性的影响,因此酶处理不受污染物本身和水中其他有毒成分的干扰,可用于高浓度、高毒性的有机废水;而对于普通的生物处理,高浓度的废水中容易导致微生物中毒,活性受到抑制。由于酶催化的高选择性,即使底物浓度很低,也同样可以维持较高的反应速率,获得满意的去除效率。因此,酶的处理效率不易受污染物浓度的影响,可在较大浓度范围内作用,且过程容易控制,基本不会产生二次污染[25]。
然而,过氧化物酶在水溶液反应中的活性通常很难长时间保持,并且通过自由基中间体或反应产物的反应容易抑制蛋白质的催化活性,在水处理的过程中容易失活,从而降低了处理效率。而且,水溶性酶属于一次性消耗品,一旦投入水中就难以将其回收利用,导致处理成本增加[25]。
过氧化物酶是催化过氧化氢氧化底物的一类酶。Yan等人研究发现三种不同粒径大小的Fe3O4 MNPs(30、50、300 nm)在H2O2存在时都可以氧化3,3,5,5-四甲基联苯胺(TMB)生成蓝色物质(OXTMB)[3]。同时他们发现这种过氧化物酶活性与颗粒大小有关,并且粒径越小活性越大。与辣根过氧化物酶(HRP)相比,Fe3O4 MNPs更稳定,它在0-90℃和pH(1-12)条件下孵化一段时间后仍能够保持较高的活性。
Gao等[3]首次发现Fe3O4磁性纳米材料具有辣根过氧化物酶的活性。Fe3O4磁性纳米材料在H2O2存在下,能够与DAB,TMB等辣根过氧化物酶的底物反应,生成与过氧化物酶相同的反应产物,从而产生与过氧化物酶相类似的催化作用。与辣根过氧化物酶相比,磁性纳米材料具有更多的酶活性优势,因为磁性纳米材料可以大批量制备,成本低,而且室温下保存更稳定,易于修饰和标记[3]。
1.2 研究目的与内容
1.2.1课题的提出
基于上述知识背景,本研究希望能通过比较三种纳米氧化铁的过氧化物模拟酶活性以及其与多种植物过氧化物酶相互之间复合作用的结果,探究纳米氧化铁在植物保护和生长调节剂的应用前景。
1.2.2研究的目的
本研究的目的是探究Fe3O4 MNPs和其他两种纳米氧化铁的过氧化物模拟酶活性以及其与几种植物过氧化物酶相互之间作用的具体方式,通过纳米氧化铁与植物中辣根过氧化物酶的正交,在H2O2存在下,与TMB反应,生成与过氧化物酶相同的反应产物,比较二者复合效果与其单独反应效果的优劣。
1.2.3研究的内容
- 不同种类纳米氧化铁的过氧化物模拟酶活性比较。
- 不同种类植物过氧化物酶活性比较。
- 纳米氧化铁与植物过氧化物酶的正交复合后的酶活性比较。
第2章实验材料和方法
2.1实验设备和试剂
2.1.1 实验设备
表2.1 仪器设备
名称 | 型号 | 厂商 |
智能人工气候箱 | HP400GS | 武汉瑞华仪器设备有限公司 |
电子分析天平 | FA2104 | 上海精密仪器仪表有限公司 |
紫外分光光度计 | UV-1601 | 上海精密仪器仪表有限公司 |
超声波清洗器 | KQ-500E | 昆山市超声仪器有限公司 |
电动低俗离心机 | TDL-5-A | 上海安亭科学仪器厂 |
2.1.2实验试剂
表2.2实验试剂
名称 | 规格 | 厂家 |
二甲亚砜 | 分析纯 | 国药集团化学试剂有限公司 |
醋酸钠 | 分析纯 | 国药集团化学试剂有限公司 |
3,3,5,5-四甲基联苯胺(TMB) | 分析纯 | 国药集团化学试剂有限公司 |
30% H2O2 | 分析纯 | 国药集团化学试剂有限公司 |
2.2 实验材料
(1)Fe3O4磁性纳米颗粒合成材料, α-Fe2O3纳米颗粒合成材料以及γ-Fe2O3纳米颗粒合成材料均购自北京化学试剂公司,使用的Fe3O4 MNPs,α-Fe2O3 NPs以及γ-Fe2O3 NPs是由水热法合成[6]。
配制(250 mg/l)Fe3O4 MNPs:用分析天平称量0.0625 g Fe3O4磁性纳米颗粒合成材料,加入250 ml去离子水中,用水热法合成得到浓度为250 mg/l的Fe3O4 MNPs,α-Fe2O3 NPs和γ-Fe2O3 NPs的配制方法同上。
(2)配制(20 μg/ml)TMB:用分析天平称量0.0001 g3,3,5,5-四甲基联苯胺(3,3,5,5-Tetramethylbenzidine, TMB),加入5 ml二甲亚砜中得到浓度为(20 μg/ml)的TMB。
(3)植物选用的是本实验室培养的拟南芥和自购的甜瓜、菠菜、小白菜。
提取拟南芥过氧化物酶:取0.12 g洗净的完整植株,加入少量PBS(pH =7.8)快速研磨至匀浆,4000 g离心10分钟后将上清全部转移并定容到10 ml得到提取酶液。甜瓜过氧化物酶,菠菜过氧化物酶以及小白菜过氧化物酶的提取方法同上。
2.3实验测定
2.3.1 纳米氧化铁的表征
②
③
①


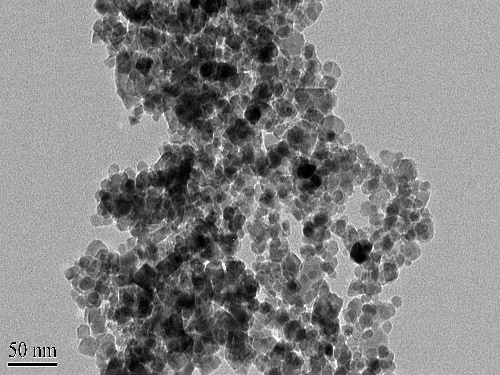
图2.1 三种纳米氧化铁的SEM图
图2.1为三种纳米氧化铁的扫描电镜(SEM)图,可以观察到其形状和粒径(①Fe3O4 MNPs;②α-Fe2O3 NPs;③γ-Fe2O3 NPs)。
2.3.2过氧化物酶(POD)活性的测定
设实验一:分别加入拟南芥过氧化物酶0、10、20、30、40、50、60 μl,编号N1~N7;
实验二:分别加入甜瓜过氧化物酶0、10、20、30、40、50、60 μl,编号T1~T7;
实验三:分别加入菠菜过氧化物酶0、10、20、30、40、50、60 μl,编号B1~B7;
实验四:分别加入小白菜过氧化物酶0、10、20、30、40、50、60 μl,编号X1~X7;
实验五:(250 mg/l)Fe3O4 MNPs的浓度梯度为6、8、10、12、14 ppm(即分别加入96μl,128 μl,160μl,196μl,228μl)分别编号a1~a5;
实验六:(250mg /l)α-Fe2O3 NPs的浓度梯度为6、8、10、12、14 ppm(即分别加入96 μl,128 μl,160 μl,196 μl,228 μl)分别编号b1~b5;
实验七:(250 mg/l)γ-Fe2O3 NPs的浓度梯度为6、8、10、12、14 ppm(即分别加入96 μl,128 μl,160 μl,196 μl,228 μl)分别编号c1~c5;
以上是毕业论文大纲或资料介绍,该课题完整毕业论文、开题报告、任务书、程序设计、图纸设计等资料请添加微信获取,微信号:bysjorg。
相关图片展示:
课题毕业论文、开题报告、任务书、外文翻译、程序设计、图纸设计等资料可联系客服协助查找。



